名古屋工業大学の研究グループは、従来過酷な条件を必要としていた「脂肪族ニトリル化合物の脱シアノ化反応」の開発に成功し、これまでにない画期的な新規合成戦略・ホウ素ラジカルの活用法を提案した(ニュースリリース)。
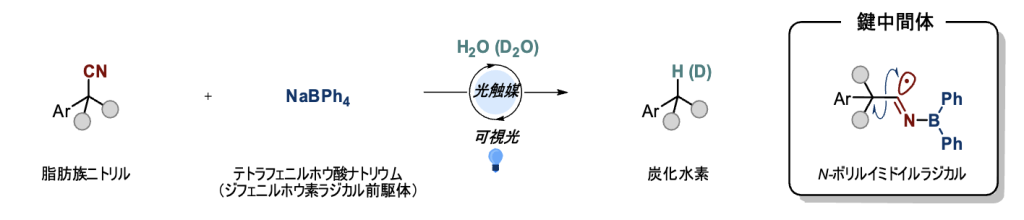
シアノ基(-CN)は強力な電子求引性を有するため、隣接炭素での脱プロトン化を伴う官能基化が容易。従って、隣接炭素上の官能基化により炭素骨格を化学修飾した後、不要となったシアノ基を脱離・変換できれば、複雑な炭化水素化合物の構築が可能となっている。
しかし、炭素-炭素結合(C–C)の開裂を伴うシアノ基の脱離反応は、結合解離エネルギーや酸化還元電位が高いため、従来法では強力な金属還元剤や遷移金属、高温・高圧条件が必要だった。このことから、環境負荷が少なく安全な条件でニトリル化合物の脱シアノ化を実現する方法の開発が強く求められていた。
研究グループは、市販のジフェニルホウ素ラジカル前駆体(テトラフェニルホウ酸ナトリウム)と脂肪族ニトリルを、光触媒存在下で可視光照射することにより、シアノ基(CN)を水素原子に置き換えることに成功した。
従来、このような分子変換を達成するには、高温・高圧条件下でラジカル開始剤を使用する必要があったが、この反応により、可視光をエネルギー源とした環境調和型の手法として、常温・常圧下での反応が可能となった。
さらに、この反応は多様な官能基を有する基質に適用可能であり、医薬品インドメタシンから調製される脂肪族ニトリルの脱シアノ化反応にも成功した。加えて、ニトリル化合物にとどまらず、イソニトリル化合物に対しても同一条件下で反応が進行し、炭素–窒素結合(C–N)の開裂を伴うイソシアノ基(–NC)の脱離を効率よく達成した。
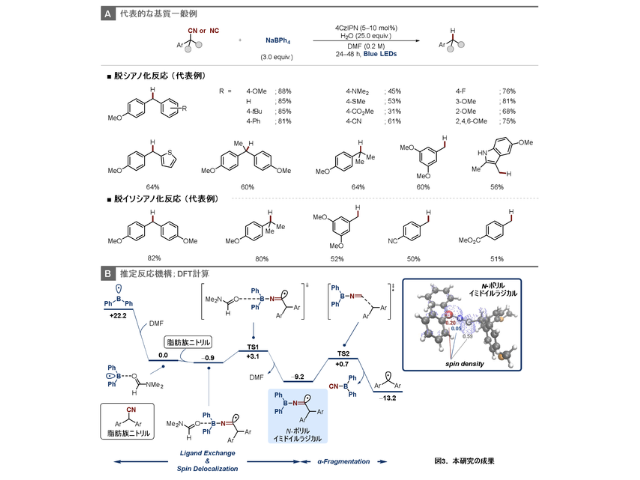
さらに、コントロール実験および密度汎関数理論(DFT)計算による反応機構解析から、反応機構を推定した。特筆すべき点は、ジフェニルホウ素ラジカルとニトリル化合物の窒素原子との配位・スピン移動により形成されるN-ボリルイミドイルラジカルの形成段階と、続くα-フラグメンテーション段階がともに、熱力学的にも速度論的にも実現可能であり、これまで活用例の少なかったジフェニルホウ素ラジカルが、この反応の高い効率に寄与している可能性が示唆された。
研究グループは、今回の成果は、ホウ素ラジカル化学の応用可能性を大きく広げるとともに、今後のシアノ基を足掛かりとした反応開発における重要な指針となることが見込まれるとしている。