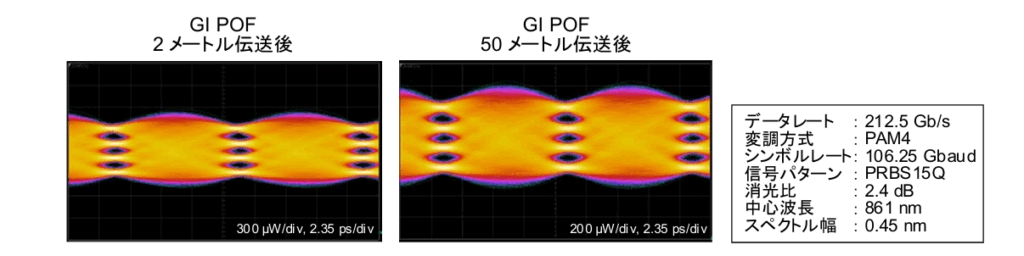
仏Institut de Biologie Structurale、兵庫県立大学、理化学研究所、高輝度光科学研究センターを含む研究グループは、ビタミンB12を用いて光を感知する光受容タンパク質CarHの活性化機構の詳細を、X線自由電子レーザー(XFEL)施設SACLAを活用した時間分解構造解析を中心に、種々の計測手法を駆使して解明した(ニュースリリース)。
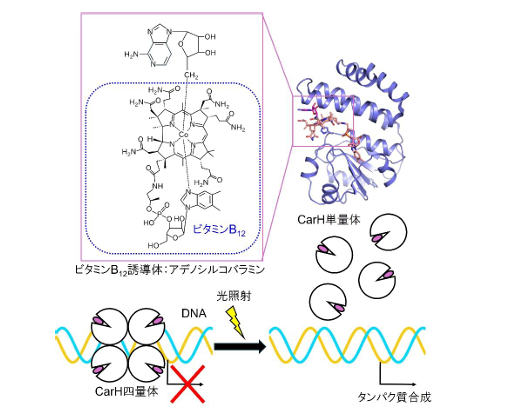
CarHは細菌にみられ、ビタミンB12を用いて光を感知し、カロテノイド合成に関わるタンパク質の合成を制御する光応答型転写調節因子のこと。CarHに結合したビタミンB12が光を受容すると、CarHの構造が変化する。その結果、四量体を形成していたCarHが単量体になることで、DNAに結合する能力を失い、タンパク質の合成が制御される。
ビタミンB12は、酵素の活性部位として機能し、生体内で様々な化学反応を行なうことがよく知られている。一方で、CarHのような光受容タンパク質において、ビタミンB12が利用される例はあまり知られていない。CarHがどのようにして「光」による機能制御を可能にしているのか、その要因は明らかになっていなかった。この疑問に答えるために、CarHが光を受けた直後のナノ秒から、最終的にタンパク質の構造が大きく変化する数秒までの「姿」をみることが重要になる。
研究グループは、主にXFEL施設SACLAでの時間分解構造解析を利用して、CarHの光活性化過程を詳細に解析した。その結果、光照射によってビタミンB12誘導体中のコバルト–炭素結合(Co–C結合)が切断された後、3マイクロ秒(マイクロ秒は百万分の1秒)で、これまで知られていなかった新しい反応中間体が形成されることを発見した。
この中間体では、光を受容する前にみられたビタミンB12誘導体中のCo–C結合(Co–C5’結合)とは異なる新たなCo–C結合(Co–C4’結合)ができており、その後に起こる大きな構造変化を引き起こす鍵となっていることがわかった。そして、CarHは四量体から単量体へ変化し、DNA結合能を失うことで転写制御が切り替わる。この仕組みは、ビタミンB12をもつ酵素とは本質的に異なる光受容タンパク質特有のものであることが示された。
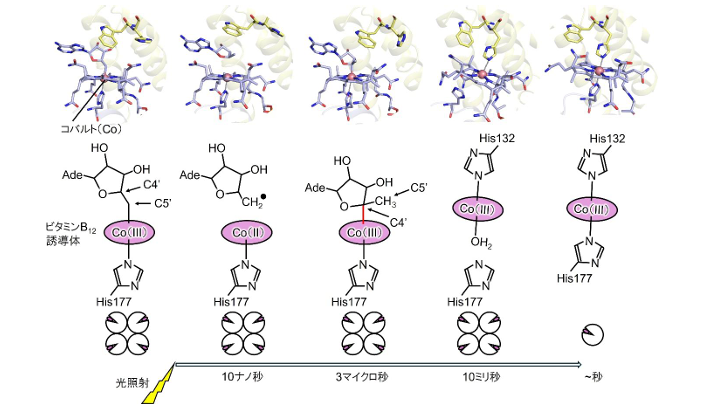
この研究は、光照射のナノ秒から数秒後のCarHの姿を捉えることで、ビタミンB12を用いた光受容の仕組みを理解した成果である。この知見は、光による遺伝子制御の理解を深めるだけでなく、将来的にはオプトジェネティクスへの応用や、光をつかってタンパク質の働きを自在に操作する技術への応用が期待される。