東京工業大学と東京大学は,新規緑色蛍光タンパク質型グルコース(ブドウ糖)センサー「Green Glifon」の開発に成功した(ニュースリリース)。
グルコース(ブドウ糖)は,さまざまな生命活動や恒常性維持において重要な役割を果たしている。細胞内グルコースの動態は,細胞内の酵素の状態や細胞外からの刺激によってダイナミックに変化し,その代謝は,さまざまな生体反応の原動力となる分子を作り出す。
グルコース動態やそれを制御する関連分子の動態を,生きた細胞内で詳しく解析するためには,蛍光タンパク質を利用した分子センサーによる生細胞イメージングが有効であり,時空間分解能および汎用性が高いセンサーの開発が待ち望まれていた。
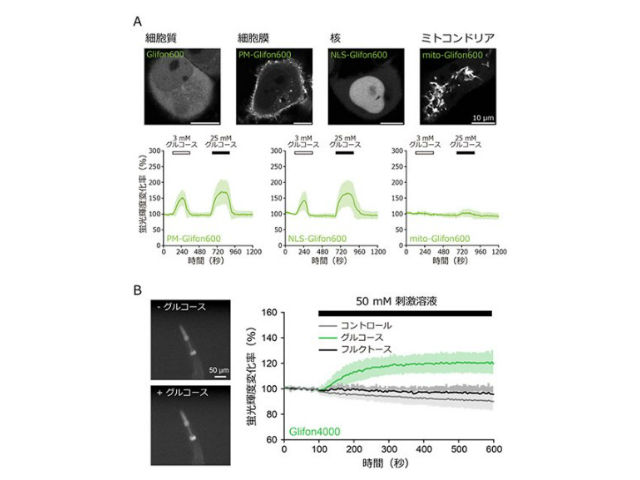
今回,研究グループは緑色蛍光タンパク質を基盤とした3種のグルコースセンサーを開発し,それらを利用した生細胞内グルコース動態の可視化に成功した。このセンサーは分割した緑色蛍光タンパク質(Citrine)の間に,グルコース結合ドメイン配列を融合した構造を持つ。
蛍光タンパク質とグルコース結合タンパク質をつなぐ,リンカー領域の長さとアミノ酸配列を最適化することにより,グルコース添加時の蛍光輝度が約7倍に上昇した。さらに,グルコース結合ドメインへ変異を導入することで,グルコースへの反応性が異なる3種の変異体を獲得することに成功した。
3種のGreen GlifonのEC50値はそれぞれ50μM,600μM,4,000μMで,これらの使い分けで生理的な濃度域である数百μM~10数mMのグルコース濃度変化のほとんどを検出できるという。
そして,細胞内のグルコース動態に加え,細胞小器官特異的な可視化やカルシウムイオンとの同時可視化も実現した。グルコースとカルシウム動態の2色同時可視化も可能であることが分かり,マルチカラーイメージングへの適用も期待できるとする。
また細胞だけでなく,線虫個体内のグルコース動態も可視化できることから,in vivoイメージングにも適用できる。さらに,人工甘味料とグルコースとの生理学的な相関を検討し,膵β細胞への人工甘味料投与が細胞内のグルコース動態を攪乱させる可能性を見出した。
以上の結果から,開発した3タイプのセンサーは生細胞のリアルタイムなグルコース動態の観察を可能にし,細胞のエネルギー動態やその破綻による病態を解析するうえで,重要なツールになるとしている。