 東京大学の研究グループは光スイッチングの可能なラマンプローブによる超解像イメージングに成功した(ニュースリリース)。
東京大学の研究グループは光スイッチングの可能なラマンプローブによる超解像イメージングに成功した(ニュースリリース)。
超解像顕微鏡は,光学顕微鏡の回折限界を克服し,ナノメートルスケールの空間分解能で生体内の細胞内構造を観察することを実現した。近年では多色超解像蛍光イメージング技術が開発されているが,蛍光は波長帯域が広いため,分離検出可能な色数が制限される。
一方,分子振動を反映するラマン散乱は,蛍光よりも50倍程度狭い線幅を持つスペクトル特性を有し,多重検出能に優れる。ラマン散乱を検出するラマン顕微鏡を用いて超解像イメージングを実現できれば,超多色・超解像イメージングの実現に有利と考えられる。
しかし,従来の超解像ラマン顕微法では高強度光の照射を必要とすることから,試料の光損傷といった問題や,複雑な光制御を必要とするなどの課題があった。
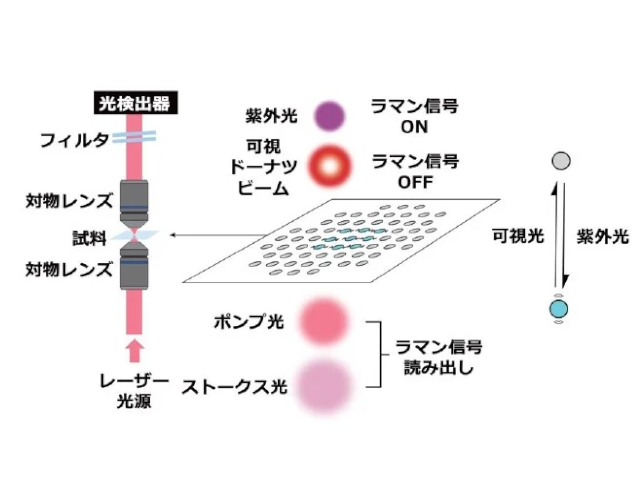
研究では,光スイッチングラマンプローブを用いる新しい超解像イメージング手法であるRESORT(REversible Saturable Optical Raman Transition)法を開発した。この手法では,高速ラマンイメージング法として知られるSRS顕微法において,微弱な紫外光と可視ドーナツビームを導入することで超解像イメージングを実現する。
RESORT法の実証のために,高いSRS信号強度を有し,光照射でラマン信号をON/OFFできる新しい光スイッチングラマンプローブDAE620を開発し,その光スイッチング特性を確認した。
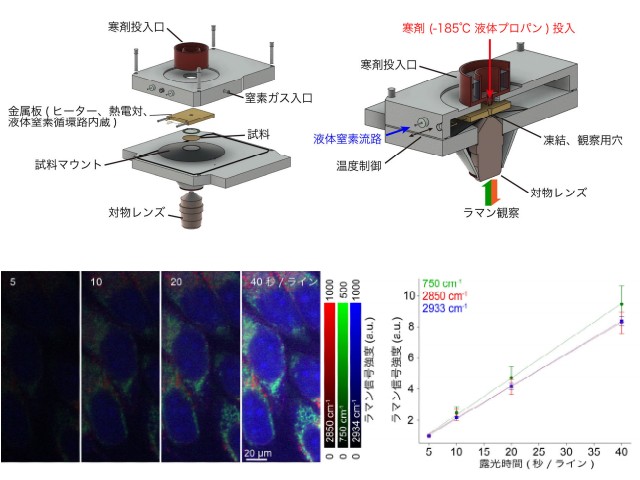
さらに,細胞中のミトコンドリアを染色可能なDAE620-mitoを合成し,ミトコンドリアの超解像イメージングを行なった。その結果,SRSイメージングでは分解できなかった構造をRESORTイメージングで分離して観察することに成功した。空間分解能は150nm程度と見積もられるという。
さらに,テスト試料を用いて空間分解能を検証したところ,可視ドーナツビームの強度を高めるとともに空間分解能が100nm程度まで向上できることがわかった。
今後,光スイッチングラマンプローブの多色展開を行ない,超多色RESORT法を実現することができれば,超多色・超解像イメージングが実現し,従来手法では観察の難しかった複雑かつ微細な生体内の構造を明らかにすることがでるとする。
研究グループは,生命の仕組みや疾病の機構の解明などにつながる新しい知見につながることが期待されるとしている。