東京大学らの研究グループは,市販の位相差顕微鏡に赤外レーザー光を照射するユニットを付与するのみで,通常の顕微画像の上に分子の空間分布画像をのせる新技術の開発に成功した(ニュースリリース)。
分子の情報を得るためには,ラマン散乱や赤外吸収を用いる手法などが知られている。しかし,ラマン散乱顕微鏡は空間分解能は高いものの感度が低く長時間の計測を要するという欠点を,また,赤外吸収顕微鏡は感度は高いものの空間分解能が低いという欠点をそれぞれ持つ。
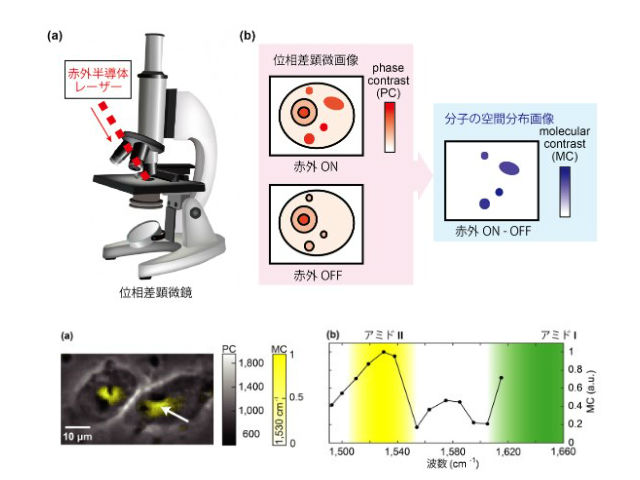
研究グループは,ラマン散乱顕微鏡や赤外吸収顕微鏡の欠点を克服する新しいラベルフリー手法「赤外フォトサーマル位相差顕微鏡」を開発した。この手法では,赤外光と可視光の照明を組み合わせることで,赤外吸収による高い感度を利用しつつ,可視光の空間分解能を実現することができる。
対象とする分子振動に対応する波長の赤外光を顕微鏡の視野内に広く照射すると,対象分子が存在する部分のみが光を吸収する。赤外光の吸収により得られたエネルギーは熱に変換され,分子の存在する位置でのみ温度上昇が誘起され,屈折率の変化が生じる。この屈折率の変化を可視光の位相変化として定量することで,可視光の高い空間分解能での分子振動の画像化を実現するという。
また,照射する赤外光の波長を変えて分光計測をすることで,複数種類の分子振動を観ることができる。今回の研究では,可視光による位相計測に市販の位相差顕微鏡を用いたが,デジタルホログラフィーなど,他の手法を用いることもできる。
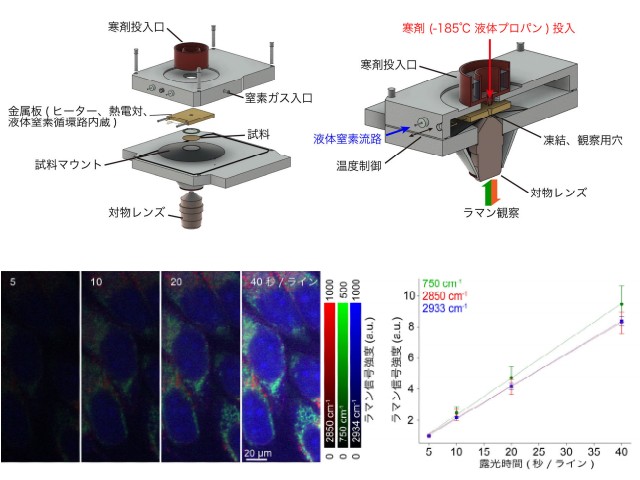
開発した顕微鏡を用いて,HeLa細胞(ヒト子宮頸がん由来の培養細胞)内の分子の分布を観る原理検証実験を行なった。タンパク質分子に含まれるペプチド結合の分子振動に共鳴する赤外光(6.5μm,1,530cm-1)を用いることで,HeLa細胞中の核周辺に存在するタンパク質の分布を可視化することに成功した。また,赤外光の波長を掃引することで空間の各点における赤外吸収スペクトルの取得を実現した。
赤外吸収スペクトルを解析することで,混合化合物中の化学組成を同定することが可能となる。今回の実験では,細胞内で約1度の温度変化を誘起し,それに伴う位相変化を検出した。
この赤外フォトサーマル位相差顕微鏡は,波長が長くエネルギーの低い赤外光と,通常の顕微鏡の可視光照明条件で実装できるため,試料へのダメージを最小限に抑えることができる。特に,生物学や医学で観察対象となる生体試料の観察に利点を持つ。研究グループはこの研究により,光学顕微鏡による通常の形状観察だけでは判断できなかった病気の診断や,生命科学の基礎研究への利用が期待できるとしている。