東京大学の研究グループは,生体内で重要な役割を担うカリウムイオンに対する高性能な蛍光センサーを開発した(ニュースリリース)。
カリウムイオン(K+)は細胞内で最も豊富に存在する金属イオンであり,神経細胞の活動や筋肉の収縮などさまざまな生理現象に深く関係しているほか,その関連タンパク質は医薬品開発においても注目されている。
蛍光センサーは,K+のようなイオンや代謝産物が,生きた細胞や生物個体の中で,どのように分布,移動し,相互作用しているかを可視化できる有用な研究ツール。その開発にあたっては近年,蛍光分子とタンパク質を併用する化学遺伝学的アプローチが注目されているが,この手法は現在のところ,カルシウムイオンなど限られた標的にしか適用されていない。
K+については,細胞や組織中での局在化が可能で,イオン選択性が高く,長波長領域で高い蛍光応答を示すセンサーは報告がなく,これらの条件を満たした新たなセンサー開発が求められていた。
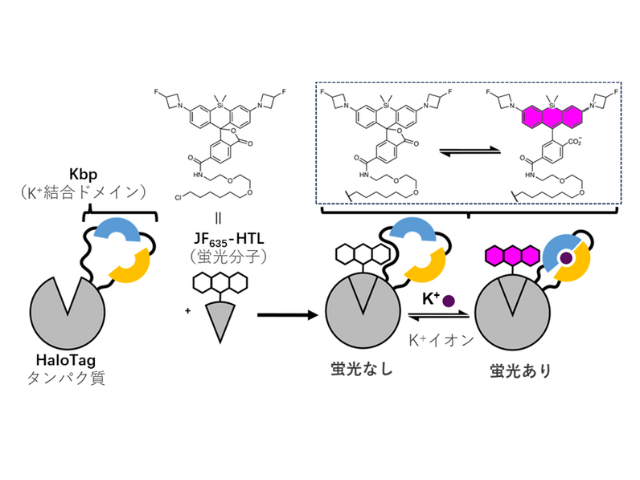
そこで研究グループは,HaloTagタンパク質を基本骨格とする化学遺伝学K+センサーの開発によって上記の課題を解決することに取り組んだ。
まず,K+の結合ドメインとして知られる細菌由来のK+結合タンパク質(Kbp)をHaloTagタンパク質中の32箇所に挿入した。そして,これらのタンパク質に対して,HaloTagと選択的に結合できる遠赤色蛍光分子JF635-HTLを結合させ,K+依存的な蛍光変化を測定した。
その結果,K+添加によって蛍光強度が88%増加する変異体が同定された。続いて,タンパク質への変異導入と性能評価を繰り返すことで,K+による蛍光増加をさらに大きくした。最終的に得られた3つのセンサーはK+添加によって最大約30倍の選択的な蛍光増加を示した。
これら3つの変異体はK+に対して異なる親和性を持つため,状況に応じて使い分けができる。また,タンパク質の結晶構造解析も行なった。K+が結合している場合,Kbp中の1本のαヘリックスの双極子が,K+と蛍光分子とを結ぶ橋として機能し,センサーの機能に重要である可能性が推測されるという。
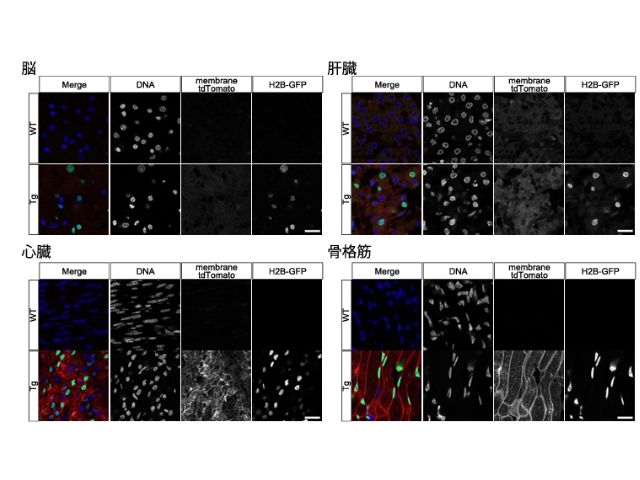
続いて,HaloKbp1シリーズをHeLa細胞に発現させてK⁺イメージングを行なった。K+の添加によってHaloKbp1シリーズの蛍光は大きく上昇し,細胞内でもK+センサーとして機能することが確認された。さらに,このセンサーが遠赤色であることを活かし,既存の緑色K⁺センサーと組み合わせた多重イメージングも実現した。
研究グループは今後,このセンサーの生物学・医学研究,医薬品候補化合物の評価などへの応用が期待されるとしている。