 北海道大学とイムラ・ジャパンは,シリコン薄膜太陽電池内に閉じ込めた光とプラズモンとの相互作用を巧みに利用して周囲の屈折率変化に対して鋭敏に電子信号を変化させる新しい原理を見出し,太陽電池とプラズモンとを結合させた革新的バイオセンサーの開発に成功した(ニュースリリース)。
北海道大学とイムラ・ジャパンは,シリコン薄膜太陽電池内に閉じ込めた光とプラズモンとの相互作用を巧みに利用して周囲の屈折率変化に対して鋭敏に電子信号を変化させる新しい原理を見出し,太陽電池とプラズモンとを結合させた革新的バイオセンサーの開発に成功した(ニュースリリース)。
アレルギー検査や癌マーカー検査,あるいはインフルエンザ検査などは,タンパク質の抗原-抗体反応を利用して検出する。
表面プラズモン共鳴(SPR)は,抗体の結合に基づく金表面のわずかな屈折率変化を検出することで,低分子数のタンパク質を定量的に測定することができ,すでにSPRセンサーとして実用化されている。
SPRセンサーは,一般的に複雑な光学的検出を介して計測されるため,比較的大型の装置を要する。そこで,SPRの精度や感度を保持したまま,電気的な検出による装置の小型化が求められてきた。
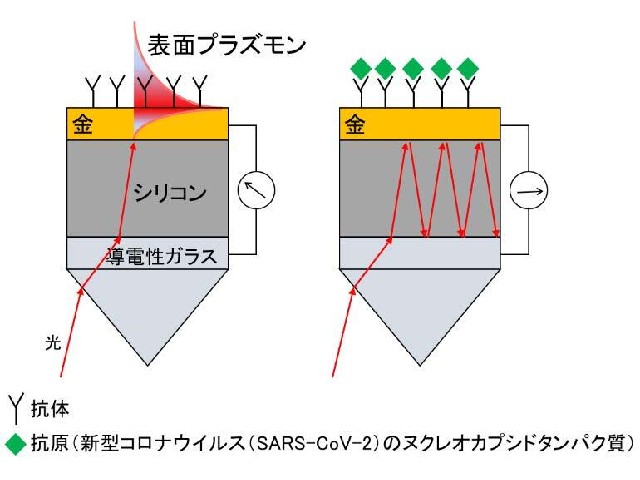
一般的にSPRセンサーは金を成膜したガラス基板にプリズムを接着したものが用いられりが,研究では導電性であるITOガラス基板上にシリコンを任意の厚みで成膜して,その上に金の薄膜を成膜することにより,シリコン内部で生じた光キャリアにより光電流として電気検出ができる仕組みとした。
その他は一般的なSPRセンサーと同様で,ある角度から光を入射するとSPRが誘起され,金表面にあらかじめ抗体を化学修飾させておき,抗原である新型コロナウイルス(SARS-CoV-2)のタンパク質を抗原-抗体反応させると金表面の屈折率が変化し,SPRの共鳴角度が変化する。
ある光の入射角度においてSPRを誘起させると光はSPRの励起に利用されるために金表面を反射せずシリコン膜内に光が閉じ込められなくなることから,得られる光電流値は小さくなる。
一方,抗原-抗体反応が進行して金表面の屈折率が変化すると共鳴条件が変わってSPRが誘起されなくなり,シリコン膜内を光が往復することにより光電流値が増幅して,新型コロナウイルスのタンパク質を電気的に検出することができることが明らかになった。これにより,タンパク質の抗原-抗体反応を利用するSPRバイオセンサーが小型な装置で実現されるという。
開発したセンサーはSPRの励起にプリズムを用いるが,センサー表面に規則的に配列したナノグレーティング構造を配置することによってもSPRを励起できることから,研究グループは,将来的にはLEDによるSPR励起と集積可能な電気検出を組み合わせたウェアラブルなバイオセンサーにも応用が期待されるとしている。