東京大学の研究グループは,第5のがん治療方法として期待されるホウ素中性子捕捉療法(BNCT)の適用範囲拡大につながる薬剤として,光で薬物動態を制御できるドラッグデリバリーシステム(DDS)を開発した(ニュースリリース)。
熱中性子とホウ素原子(10B)の核反応によりがん細胞を殺傷する治療法であるBNCTの適用範囲拡大の鍵を握るのはホウ素薬剤で,現在唯一承認されているのはボロノフェニルアラニン(BPA)という薬剤。BPAはLAT1というがん細胞で多く発現しているアミノ酸トランスポーターを介して細胞に取り込まれるため,がんに選択的に集積することができる。
しかしながら,LAT1の発現量が少ないがんなどに対しては必ずしも十分に集積できないことがあり,そのようながんに対して選択的に集積できる新たな薬剤が必要とされている。
これまでの研究では高分子ミセルやリポソームなどのDDSを用いて,EPR効果を利用して薬剤を腫瘍に選択的に送達する試みが行なわれてきた。
しかし,そのような従来のDDSは,高いがん集積性を得る前提として薬剤が長期的に血中に滞留する必要があった。その結果,がんに集積しなかった多くの薬剤は,血液中に残存してしまい,熱中性子照射時に正常組織でも核反応が多く生じ,副作用につながる懸念があった。
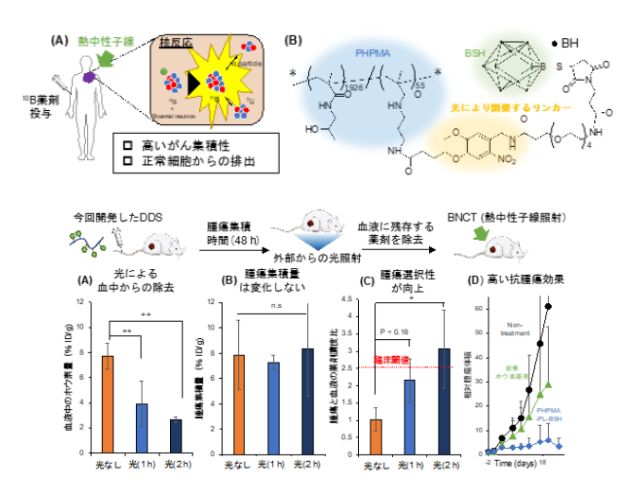
この問題を解決するため研究グループは,がんに集まらずに血液中に残存してしまった薬剤を,光を利用して速やかに除去できるDDSを開発した。このDDSは,生体適合性高分子poly(2-hydroxypropyl methacrylate)(PHPMA)誘導体の側鎖に,単剤では即座に腎排泄される低分子ホウ素薬剤(BSH)を,光によって開裂するリンカーを介して結合した構造を持つ。
マウス皮下腫瘍モデルにおいて,静脈注射されたこのDDSは高い血中滞留性により腫瘍に効率的に集積する。その後,腹部にLEDで光を当てると,血液中に残存してしまったDDSから低分子ホウ素薬剤が切り離され,速やかに尿として排出される。
その結果,臨床に求められる腫瘍選択的集積と血中からの速やかな除去を実現することができた。同モデルにおいて臨床の条件を模倣してBNCTを行なうと,従来の薬剤と比較して有意に優れた治療効果が得られた。
研究グループは,光で薬物動態を制御する今回の研究成果により,BNCTの適用範囲拡大につながることが期待されるとしている。