 京都大学の研究グループは,リンイリドと二種類のアルケンを炭素-炭素結合形成反応によって逐次的に連結し,医薬品などの合成に有用な1,4-ジカルボニル化合物を迅速に供給する新しい手法を開発した(ニュースリリース)。
京都大学の研究グループは,リンイリドと二種類のアルケンを炭素-炭素結合形成反応によって逐次的に連結し,医薬品などの合成に有用な1,4-ジカルボニル化合物を迅速に供給する新しい手法を開発した(ニュースリリース)。
複雑な構造を有する医薬品を合成する場合,結合形成反応を何度も繰り返しながら複数の構成要素を一つずつ繋げていく必要があるため,連続反応によって複数の分子を簡便かつ迅速に連結する手法が精力的に研究されてきた。
これらの分子は,自身と複数の化合物の間で次々と結合を形成し,一つの最終生成物を与える。これら一連の反応が一つの反応容器中で進行するため,中間体の単離・精製といった過程を経ることなく,効率的に複雑な骨格をもつ分子が得られる。
しかし,分子連結素子のほとんどは,結合形成の過程で高い反応性を有する有機金属化学種を用いる必要があり,これらと反応する官能基は使えないことや,一般に不安定な有機金属試薬の取り扱いに専門的な知識と技術を要することが課題だった。
研究グループは,こうした課題を克服するため,反応性化学種の一つであるラジカルを利用する連続反応に着目した。
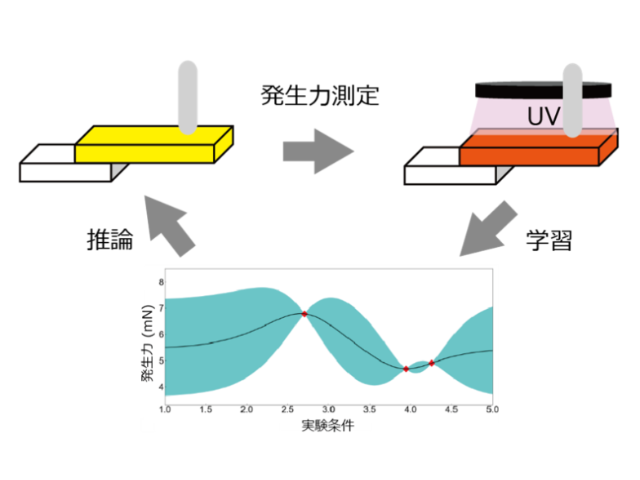
今回の反応では,穏和な条件下でラジカル種を発生させる手法として,再生可能エネルギーである可視光を駆動力とする光レドックス触媒を使用した。目的の連続反応の開発に先立ち,リンイリドの光レドックス条件下における反応性を調べたところ,以下のような実験結果を得た。
① ホルミル基をもつリンイリドに光レドックス触媒を作用させると,求核的な性質を有する炭素ラジカルが発生し,これが電子不足アルケンに付加することで中間体を与えた。
② ①で得られた中間体に対し,シュウ酸と共触媒を加えた上で同様の光レドックス触媒を作用させると,リン原子を含む部位の脱離を経て求電子的な炭素ラジカルが発生しこれが電子豊富アルケンに付加することで目的物を与えた。
これらの結果は,用いたリンイリドが求核性および求電子性という二面性をもつ炭素ラジカルとして振る舞うことで,性質の異なる二つのアルケンを繋ぎとめる役割を果たすことを示している。
そこで,これらの結果をもとに反応条件を精査し,①,②の反応を一つの反応容器内で逐次的に進行させる条件へと最適化することで,リンイリドを新たな分子連結素子とする連続ラジカル反応を達成した。
従来法をはるかに凌ぐ高い官能基許容性は,これまで合成が困難であった多様な類縁体の供給にも繋がることから,研究グループは,創薬研究における医薬品探索の高速化へ貢献できるとしている。