 東北大学の研究グループは,コニカミノルタと共同で,がんの診断や治療の標的となるタンパク質の量を,感度・精度良く定量的に検査する方法の開発に成功した(ニュースリリース)。
東北大学の研究グループは,コニカミノルタと共同で,がんの診断や治療の標的となるタンパク質の量を,感度・精度良く定量的に検査する方法の開発に成功した(ニュースリリース)。
がんの組織診断では,診断や治療の指標となる様々ながん関連タンパク質の量を調べる事が必要。そのため,手術前の生検や手術で摘出したがん組織において,免疫組織化学法でタンパク量を算出する。現在,免疫組織化学法として発色の濃さでタンパク質の量を定量するDAB染色と呼ばれる方法が主流だが,この方法はタンパク量の定量性に問題があった。
これを解決する方法として,蛍光色素を使った組織診断法(蛍光免疫染色法)が開発されてきたが,組織は強い自家蛍光を発するため,蛍光免疫染色法にも限界があった。
東北大では,この課題を解決するため,市販されている蛍光ナノ粒子と独自の光学装置および画像解析を組合せた「蛍光ナノ粒子の1粒子イメージング法」による組織診断法を2015年に開発した。この方法で,標的タンパク質の数を定量的に評価することに成功したが,検出感度については格段の向上は認められなかった。
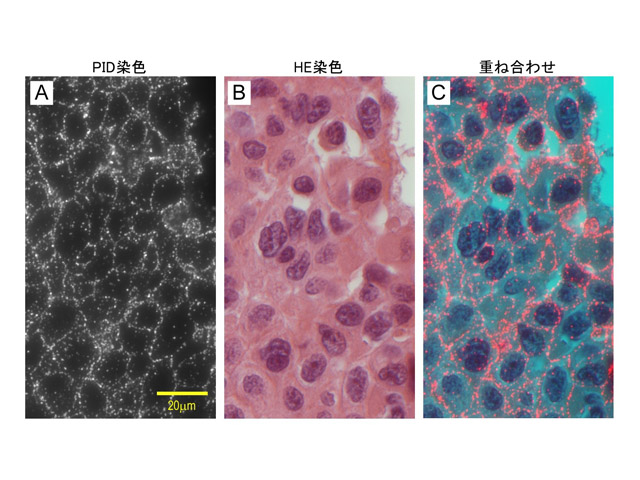
さらに,がん組織診断では,HE染色によって細胞の形態を同時に観察することが不可欠だが,HE染色に使用するエオシンは強い自家蛍光の原因となるため,蛍光ナノ粒子染色とHE染色を同時に用いて性状と形態の両面から診断することは困難だった。
今回,課題を解決するため,「東北大学の蛍光ナノ粒子の1粒子イメージング技術」と「コニカミノルタの材料合成技術」とを融合した新しい蛍光染色法を開発した。研究グループは,蛍光色素の1つであるペリレン色素に着目し,強い蛍光を得るために,この蛍光色素を約10万分子含んだナノ粒子を合成した。さらに,このナノ粒子に従来の免疫組織化学法が流用できるような修飾を施し,PID(Phosphor-Integrated Dots)粒子と命名した。
PID粒子は市販の蛍光ナノ粒子に比べ100倍以上明るく,組織の自家蛍光の影響を全く受けることなく蛍光シグナルを検出することができた。また,組織画像のPID粒子数を算出するため,独自の解析アルゴリズムを開発した。従来の染色法と比較した結果,PID粒子染色法は他の方法に比べ,検出感度が 300倍以上に改善した。さらに,PID粒子は細胞のタンパク質発現量を定量的に測定可能であることも分かった。
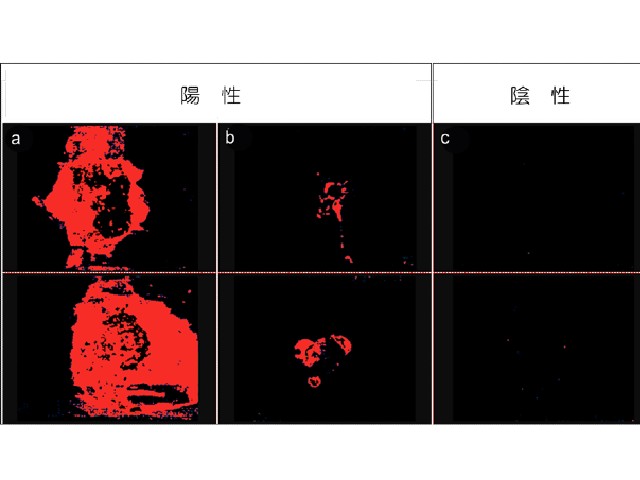
近年,乳がんでは,HER2を標的とした抗がん剤の1つであるトラスツズマブを,HER2陽性の患者に対し,手術前の薬物療法として使用しているが,患者によって薬効を事前に予測できないことが課題となっていた。そこで,PID粒子染色法を適用し,がん組織に存在するPID粒子の数とトラスツズマブの奏功性を比較した結果,従来の方法に比べ,トラスツズマブの奏功性を明瞭に判別し,がん分子標的薬の効果をより良く予測できた。
さらに,PID粒子は蛍光が非常に強いため,がん組織のHE染色による細胞形態の観察とPID粒子による細胞性状の蛍光染色を,同一の組織切片を用いて行なうことを可能としした。
この研究の成果から,PID粒子を用いた診断法は,がん分子標的薬の薬効を投薬前に高い精度で診断できることが示された。これは,がん分子標的薬の効果が低いと予想された場合は,異なる抗がん剤を選択することを可能とする。この方法は将来的に精密医療(プレシジョン・メディシン)へ貢献すると期待されるとしている。