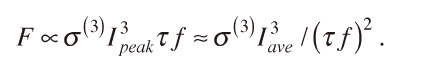1. はじめに

超解像顕微鏡1〜3)や多光子顕微鏡4, 5)を含む様々な蛍光顕微鏡が開発され,生命現象解明のための重要な技術になっている。しかし,空間分解能,観察可能な深さ,時間分解能,視野の広さがトレードオフの関係にあるため,脳組織などの生体組織深部のイメージングにおいて,イメージング性能が足りていない。例えば,超解像顕微鏡は回折限界を超えた空間分解能を達成できるが,試料の表面近傍しか観察できない。この理由は,微弱な信号光が背景光に埋もれやすいためである。
近年,上記のトレードオフの関係を打破するための技術が開発され始めている。例えば,レーザー走査を行わずに,広視野の多光子蛍光断層像を取得できる時空間集光顕微鏡がある6)。時空間集光顕微鏡を用いると,サブミクロンの面内方向の分解能,数ミクロンの深さ方向の分解能で,広い視野(5000−20000μm2)のビデオレートイメージングができる7, 8)。また,別の例として,超解像顕微鏡と多光子顕微鏡を組み合わせることによって,深部イメージングにおける空間分解能を向上させることも可能になっている9〜12)。本稿では,時空間集光顕微鏡技術を紹介するとともに,時空間集光顕微鏡と超解像顕微鏡を組み合わせた干渉時空間集光顕微鏡12)について紹介する。
2. 時空間集光顕微鏡
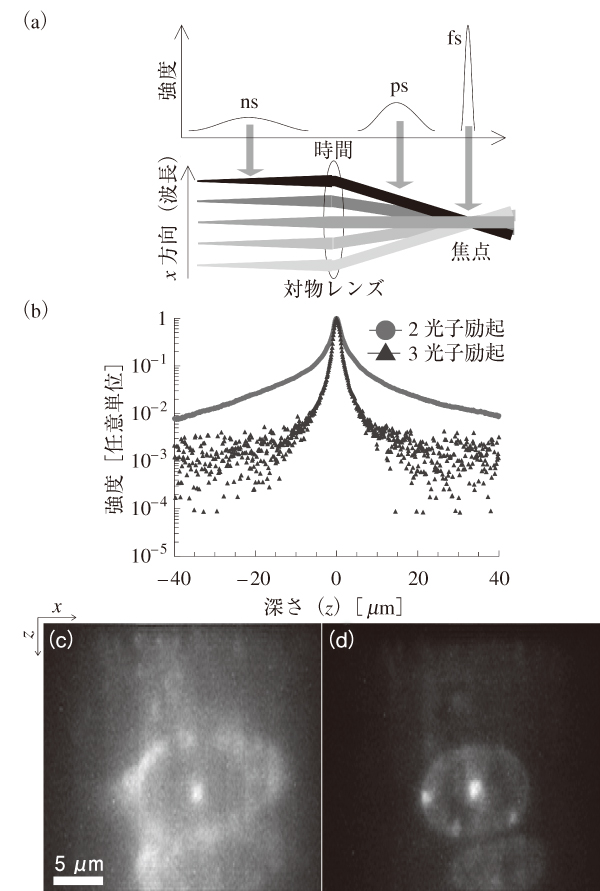
時空間集光顕微鏡では,図1(a)に示すように,フーリエ変換限界のフェムト秒のレーザーパルスを回折格子などの分散素子によって分光し,対物レンズによって試料内部へと集光する6)。スペクトル成分が空間的に分光されることによって,パルス幅がナノ秒やピコ秒に拡がるが,焦点面に近づくにつれて空間的に重なるスペクトル帯域幅が拡がるため,パルス幅が短くなっていく。焦点面では全てのスペクトル成分が空間的に重なるため,フーリエ変換限界のフェムト秒のパルス幅に戻る。
その結果,高い励起光強度を必要とする多光子吸収過程が誘起される領域は,ピーク強度の高くなる焦点面近傍に局所化される。このとき,ビームを回折限界まできつく空間集光する必要はなく,広視野を照明する面照射を用いたとしても,励起領域は焦点面近傍に局所化される。面照射を用いれば,焦点面を共役な位置に配置されたカメラに結像することによって,レーザー走査を一切行うことなく,広視野の多光子蛍光断層像を取得できる。そのため,時空間分解能と視野の広さとのトレードオフの関係を打破できる7, 8)。
我々は,2光子励起を用いた時空間集光顕微鏡における深さ方向の励起領域をさらに局所化するために,3光子励起を用いた時空間集光顕微鏡を開発してきた13)。ここで重要となるのが,光褪色や光損傷を抑制可能な3光子励起用の最適な光源である。2光子吸収断面積が10–49 cm4s/photonであるのに対して,3光子吸収断面積σ(3)は10–83 cm6(s/photon)2と非常に小さい。そのため,3光子吸収を誘起するためには,2光子吸収を誘起するよりも非常に高い励起光強度が必要である。
しかし,市販の2光子顕微鏡に搭載されるパルス幅200 fs,繰返し周波数80 MHzのフェムト秒レーザーでは,ピーク強度が足りないために,試料表面の観察でさえ,試料に入射させる平均パワーを数100 mWまで高くする必要がある。高い平均入射パワーは,水の1光子吸収に伴う温度上昇などによって,試料に損傷を与えてしまう。この問題を避けるために,我々は,パルス幅92 fs,繰返し周波数200 kHzのファイバー増幅器を作製した。3光子蛍光強度Fは式(1)で示されるように,平均強度Iaveが一定の場合に,パルス幅τと繰返し周波数fの2乗に反比例する。
したがって,市販の2光子顕微鏡に搭載されるフェムト秒レーザーに比べて,作製したファイバー増幅器では,同じ平均入射パワーでも,3光子蛍光強度を7.5×105倍高くすることが可能である。また,繰返し周波数を下げることによって,蛍光分子の光褪色も抑制できる14)。多光子励起における光褪色には,蛍光分子が1つ目のパルスで励起され,3重項状態へ遷移した後,2つ目のパルスでさらに高いエネルギー状態へと励起され,光褪色する過程がある。
図1(b)に示すように,深さ方向の励起領域を2光子励起よりも局所化することに成功した。この効果は,図1(c),(d)に示すように,核をDAPIとSYTO83によって二重染色したマウスの脳組織のイメージング結果において,背景蛍光が抑制されていることからも確認できる。