九州大学,東京医科歯科大学,神奈川県立産業技術総合研究所は,生体透過性が高い赤色・近赤外光を生体内で青色光に変換可能なフォトン・アップコンバージョン(UC)ナノ粒子を開発し,生体内で神経細胞を光操作することに成功した(ニュースリリース)。
生体組織への高い透過性を示す赤色光や近赤外光を青色光に変換するUC技術が近年注目を集めている。アップコンバージョンにはいくつかの機構が存在するが,特に有機分子の三重項-三重項消滅に基づくアップコンバージョン(TTA-UC)は他の機構よりも弱い強度の光を変換可能であるという点でより実用的と言える。
UC材料は,体外から照射された赤色光を生体内で青色に変換することで,侵襲性の低い生体内青色光源として機能する。これまでにUC材料を用いた生体外/生体内オプトジェネティクスが実証されてきたが,生体毒性の懸念がある重金属材料を含むことが課題だった。
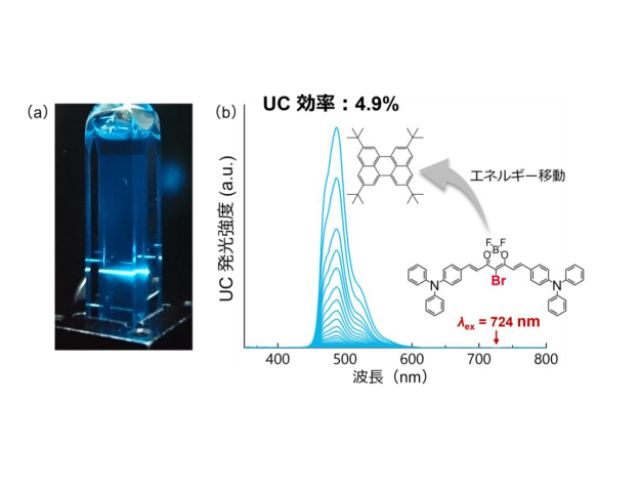
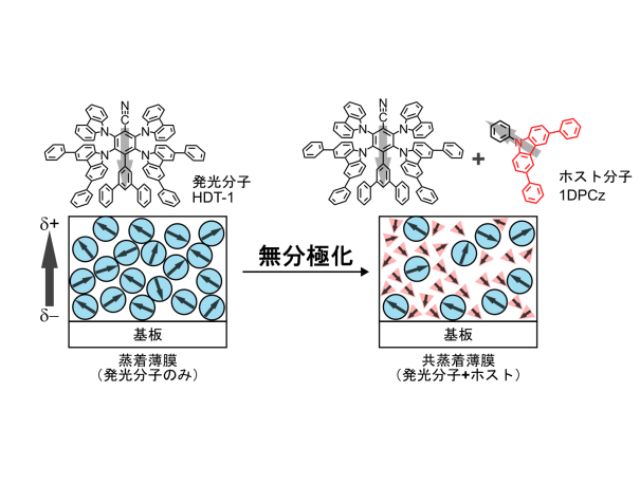
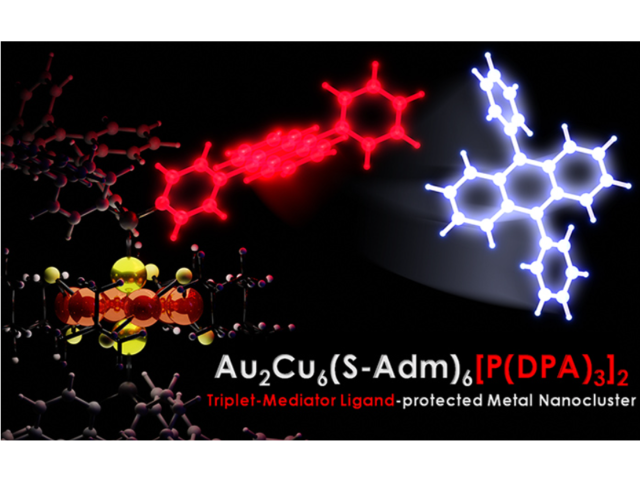
今回の研究では,重金属を含まない有機フォトン・アップコンバージョンナノ粒子を用いた生体内オプトジェネティクスを初めて実証した。重金属を含まない新規三重項増感剤として,ブロモ基を有する熱活性化遅延蛍光(TADF)材料を設計した。
有機TADF増感剤にブロモ基を導入することで,重原子効果により励起一重項状態から励起三重項状態への系間交差(ISC)効率が促進され,UC効率が大幅に向上した。
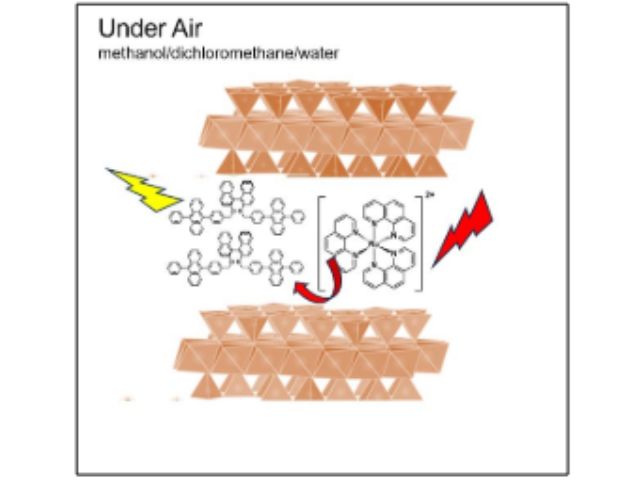
開発した重金属フリーのUC材料を用いて,水中油型UCナノ粒子を開発した。UCナノ粒子は高い生体適合性,水分散性,酸素耐性を有し,空気中で安定なUC発光を示す。UCナノ粒子を生体内オプトジェネティクスへ応用するために,青色光応答性PA-Cre技術を利用した。
PA-Creは東京大学が開発したタンパク質で,青色光照射下でDNA組換え酵素Creが活性化する技術。研究グループは,Creの活性化で緑色蛍光タンパク質EGFPが発現誘導されるシステムを用いて生体内オプトジェネティクスを検討した。
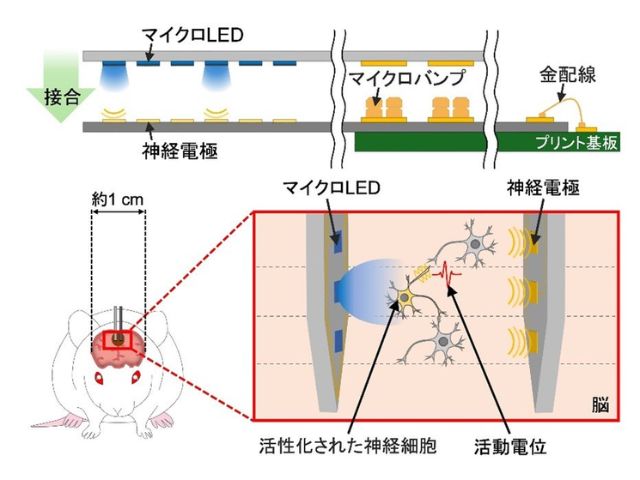
新生仔マウスの大脳皮質神経細胞でPA-Creを発現させ,隣接する領域の皮下にUCナノ粒子を投与し,体外から赤色光を照射した。その結果,生体内でUCに基づく青色光が生じ,PA-Creの活性化によるEGFP発現の誘導に成功した。
研究グループは,今回の成果により,生体内の神経活動を低侵襲的に光操作できるようになり,オプトジェネティクスによる生命・医療分野への展開が期待されるとしている。