東北大学と綜研化学は,高分子の相分離と静電相互作用を用いた自己組織化プロセスにより,高い光学密度をもつコンポジット微粒子(GNDP)を作製し,そこにインフルエンザ抗原に対する抗体を結合すること,抗原を高感度に検出できる検出プローブとなることを見出した(ニュースリリース)。
インフルエンザや新型コロナウィルスなどの抗原検査として一般的なイムノクロマト法は,プローブとして検出抗体を結合した金ナノ粒子を用いる。しかしながら金ナノ粒子は数nm〜数10nmと小さく,光学断面積が小さいため,検出には大量の粒子が必要となる。
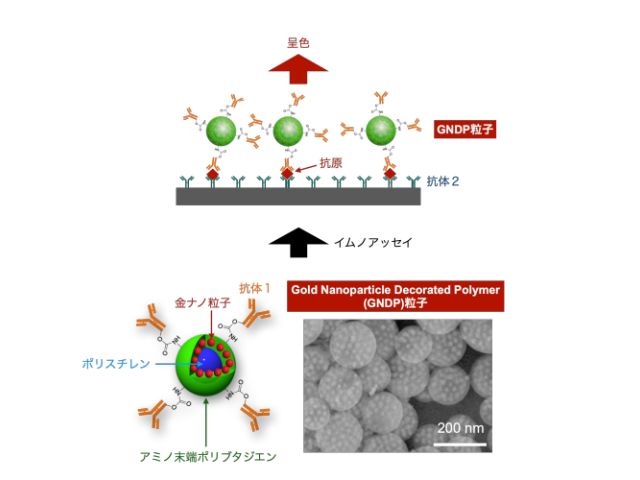
これまで研究グループは,高分子を有機溶媒に溶かした溶液に高分子の貧溶媒を加え,良溶媒を蒸発除去することで高分子微粒子を得る自己組織化析出(SORP)法を独自に開発し,極性高分子と非極性高分子を混合した溶液からコアシェル型の高分子微粒子が得られること,極性高分子にアミノ基など電離可能な官能基が存在すると粒子が正に帯電すること,さらにその水分散液に負に帯電した金ナノ粒子を加えると,静電相互作用により金ナノ粒子がコアシェル型高分子微粒子の表面に吸着し,密に配列して水中に分散可能なコンポジット微粒子(GNDP粒子)が得られることを見出していた。
今回研究グループは,アミノ末端ポリブタジエン(PB-NH2)とポリスチレン(PS)からなるコアシェル型粒子をSORP法により作製した。得られたコアシェル型粒子はPSがコア,PB-NH2からなるシェルを持ち,PB-NH2のアミノ基により,中性付近の水中で正に帯電する。
そこに,5nm,10nm,20nmの粒径を持つ負に帯電した金ナノ粒子を混合することで,各金ナノ粒子が表面に密に配列したGNDP粒子を作製した。吸光度を比較したところ,20nmの粒径を持つ金ナノ粒子をコンポジット化したGNDP粒子が大きな吸光度を持ち,かつ分散性を維持していることがわかった。
このGNDP粒子と市販のELISA用インフルエンザキットを利用し,検査プレートとGNDP粒子の表面にインフルエンザ抗原に対する抗体を結合させ,サンドイッチアッセイを行なうことにより,GNDP粒子がインフルエンザ抗原検出のプローブとして応用可能か検証を行なった。
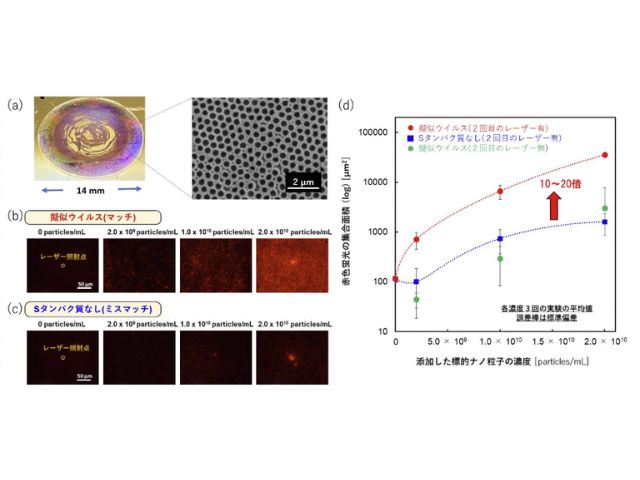
その結果,GNDP粒子は抗原濃度に対する感度が通常のELISAアッセイに使用される呈色剤や金ナノ粒子と比較しても高く,金ナノ粒子単体では測定が難しい低濃度領域でもアッセイ可能なことが示された。
研究グループは,抗原量の定量測定や,さまざまな疾病マーカーを高感度に検出する新たなプローブ粒子としての利用が期待される成果だとしている。