基礎生物学研究所/生命創成探究センター(ExCELLS)と仏国立科学研究センターは,細胞周期進行に重要な働きを果たすキナーゼ(リン酸化酵素)であるCDKの活性をリアルタイムに1細胞レベルで可視化するバイオセンサー(Eevee-spCDK)を開発し,CDKの活性がある閾値に達したときに細胞周期進行が誘導されることを直接的に検証することに成功した(ニュースリリース)。
細胞はゲノムDNAを複製し,細胞分裂と共に娘細胞へ正確に分配する細胞周期を繰り返す。この正確な細胞周期の実現には,CDKの活性制御が重要。これまでの研究でCDKを制御する因子の役割は大部分が明らかにされたが,時間・空間分解能の制限により,リアルタイム・1細胞レベルでの解析は難しかった。
今回,研究グループは,CDKの活性によって蛍光特性が変化するようなバイオセンサーを新たに設計した。このバイオセンサーを分裂酵母に導入し、様々な培養条件や変異株で、CDK活性の動態を調べた。
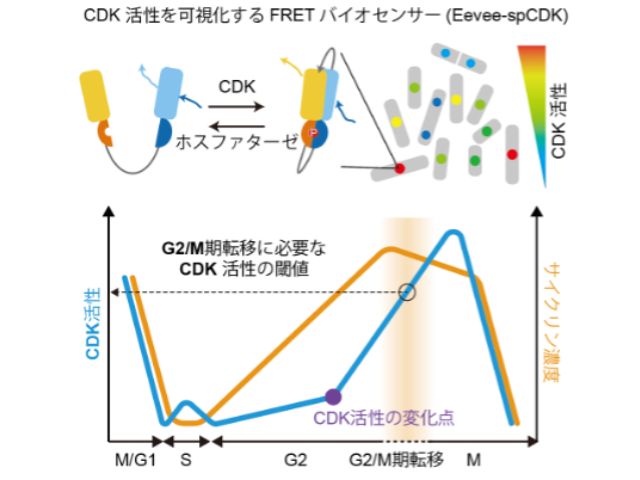
このバイオセンサーは,フェルスター共鳴エネルギー移動(FRET)と呼ばれる現象を利用したもの。活性化したCDKによってセンサードメインがリン酸化されると,リガンドドメインがセンサードメインと結合し,二つの蛍光タンパク質が近接することでFRETが起こる。
CDKによるリン酸化を効率よく受けるセンサードメインを探索するために,過去の研究から選定した14個の基質候補のうちの一つが,細胞周期の進行に伴って最大40%程度のFRET効率の変化を示すことがわかった。
また,このFRET効率の変化は,バイオセンサーのリン酸化によるものであることが確かめられた。研究グループは,このバイオセンサーをEevee-spCDKと名付けた。
Eevee-spCDKを用いて,分裂酵母の様々な変異株におけるCDK活性の変動とG2/M期転移のタイミングを計測したところ,G2/M期転移がCDK活性の閾値によって誘導されるという仮説に,直接的な実験的証拠を与えることができた。
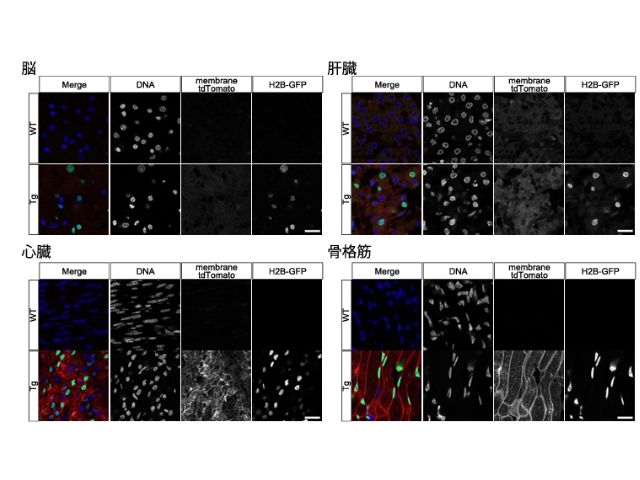
Eevee-spCDKは分裂酵母のために設計されたものだが,その応用範囲は分裂酵母に限定されず,様々な真核細胞でのCDK活性を測定する有用なツールであることが示唆された。
研究グループは,高い時空間解像度でのCDK活性の可視化への道を拓くEevee-spCDKは,CDKを通じた細胞周期の動的な制御原理を明らかにする強力な手段となることが期待できるとしている。