 神戸大学と生理学研究所は,環形動物ゴカイ由来の自己不活性化する特性を持つ光受容タンパク質を利用して,多様な細胞応答の中でイオンチャネル応答を選択的に光で制御できる「精密バイアス光操作ツール」を開発した(ニュースリリース)。
神戸大学と生理学研究所は,環形動物ゴカイ由来の自己不活性化する特性を持つ光受容タンパク質を利用して,多様な細胞応答の中でイオンチャネル応答を選択的に光で制御できる「精密バイアス光操作ツール」を開発した(ニュースリリース)。
光遺伝学解析には,これまでは微生物由来のチャネルロドプシンが細胞応答を光で操作するためのツールとしてよく用いられてきたが,最近では種々の動物が持つオプシンとよばれる光感受性Gタンパク質共役受容体(GPCR)も注目されている。
動物オプシンは,チャネルロドプシンよりも百倍〜数千倍弱い光でも細胞応答を誘起できる一方,Gタンパク質や他のシグナルタンパク質を介して,イオンチャネルがイオンを通す電気応答や酵素が細胞内の物質を変換する代謝応答など多様な細胞応答を引き起こすため,何を操作しているのか不明確になる難点もあった。
今回,環形動物ゴカイ由来のc-opsin1というオプシンが持つ,紫外光(UV)刺激によって活性化され,黄色光刺激で不活性化あるいは光刺激を止めることで自己不活性化する特性に着目した。
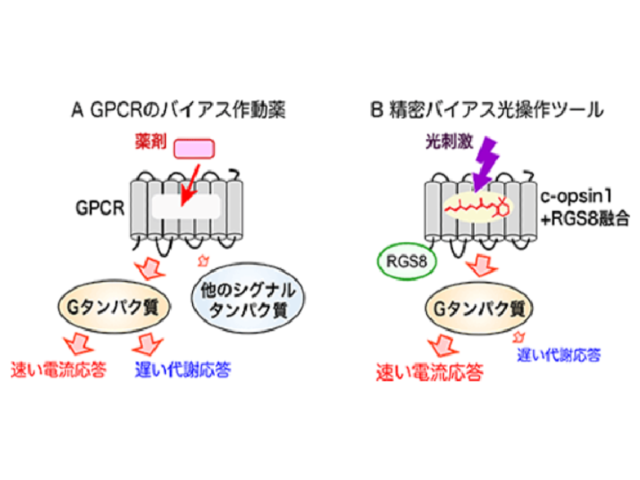
c-opsin1は不活性化するまでの短時間だけGタンパク質を活性化するため,細胞応答の中でも数秒で生じる「速い電気応答」はしっかり誘起できるが,数分で起こる「遅い代謝応答」は小さいことを発見した。つまり,c-opsin1はイオンチャネル応答と代謝応答の両方ではなく,イオンチャネル応答を「狙いうち」して光制御できることになる。
このc-opsin1が持つ特性をさらに強化するために,Gタンパク質を介した細胞応答を加速できるRGS8というタンパク質を遺伝子工学によってc-opsin1と融合させた人工タンパク質を作製し,光によって生じる細胞応答を詳細に検討した。
その結果,この人工タンパク質はもとのc-opsin1と比べて,より速いイオンチャネル応答を引き起こし,代謝応答はほぼ全く引き起こさないことを見出した。つまりこの人工タンパク質は,イオンチャネル応答を選択的かつ素早く光で駆動できる光操作ツールとしてはたらく。
言い換えれば,この新規ツールはいろいろな細胞応答を同時に駆動してしまう動物オプシンの光操作ツールとしての難点を克服した。GPCRに作用し,Gタンパク質のみあるいは他のシグナルタンパク質のみに由来する細胞応答を「狙いうち」すなわちバイアスをかけて駆動できる薬剤は「バイアス作動薬」と呼ばれ,新薬候補として注目されている。
開発した光操作ツールは,その困難さを乗り越えた「精密バイアス光操作ツール」であり,研究グループは,光遺伝学の発展やGPCRが関わる生理機能の理解につながるとしている。