 東京大学は,光照射によってアルツハイマーモデルマウスの脳内で非侵襲的にアミロイドβ(Aβ)の凝集体を低減する化学触媒の開発に成功した(ニュースリリース)。
東京大学は,光照射によってアルツハイマーモデルマウスの脳内で非侵襲的にアミロイドβ(Aβ)の凝集体を低減する化学触媒の開発に成功した(ニュースリリース)。
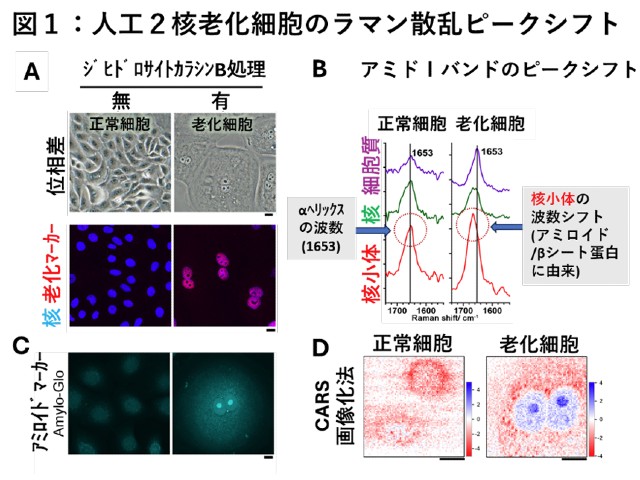
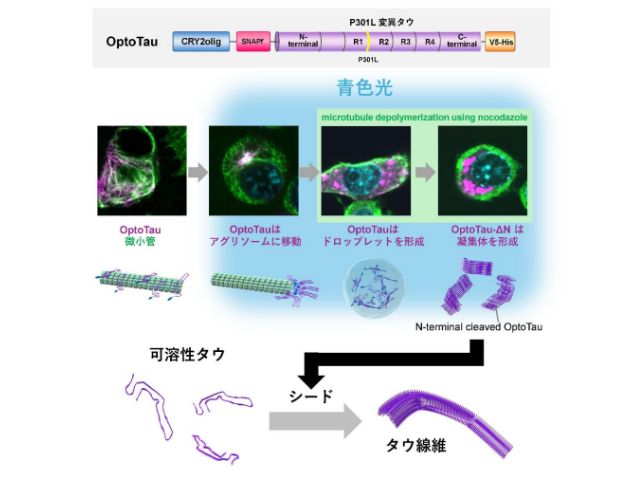
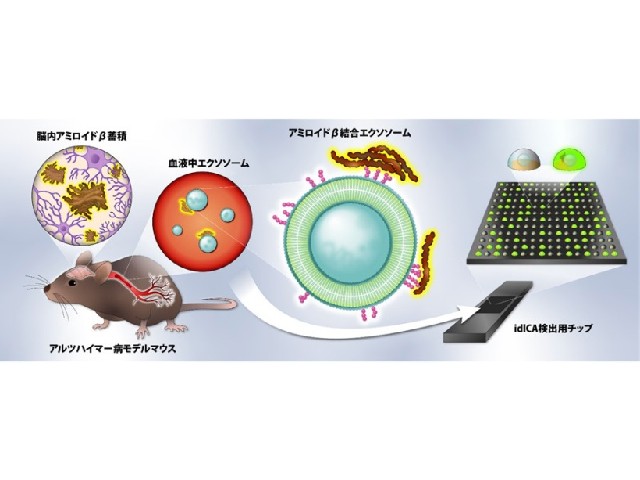
アルツハイマー病の発症には,Aβというペプチドが凝集して神経細胞を傷つけることが関わっていると考えられている。
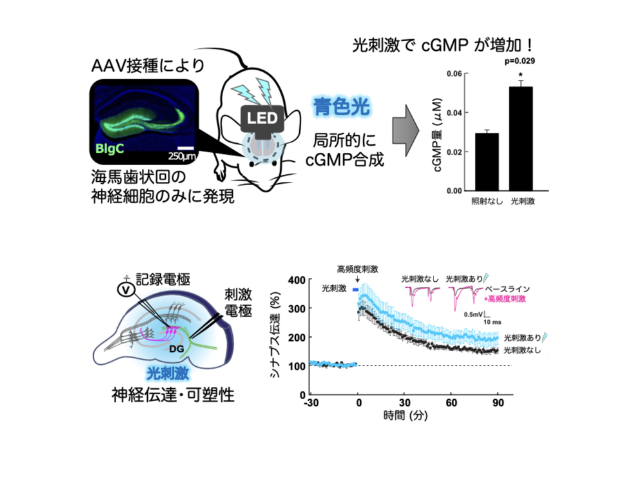
研究グループはこれまでに,化学触媒を用いた酸素化反応に基づく新しいアルツハイマー病治療法の研究を進めてきた。光照射下で触媒を作用させてAβを酸素化し,これによりAβの凝集性や毒性が抑制できることを見いだしてきた。しかし,これまでの触媒は血液脳関門を透過することができなかったため,脳内でAβを酸素化するためには,侵襲性の高い手術を伴う直接的な脳への触媒投与と光デバイスからの光照射が必要だった。
より侵襲性の低い脳内Aβの酸素化の実現を目指して研究を行なった結果,今回,血液脳関門を通過可能な全く新しい触媒を開発した。この触媒は,血液脳関門を通過できる小さい分子量の化合物であるにもかかわらず,マウスの頭蓋骨を通過するオレンジ色の光を吸収することができるという。
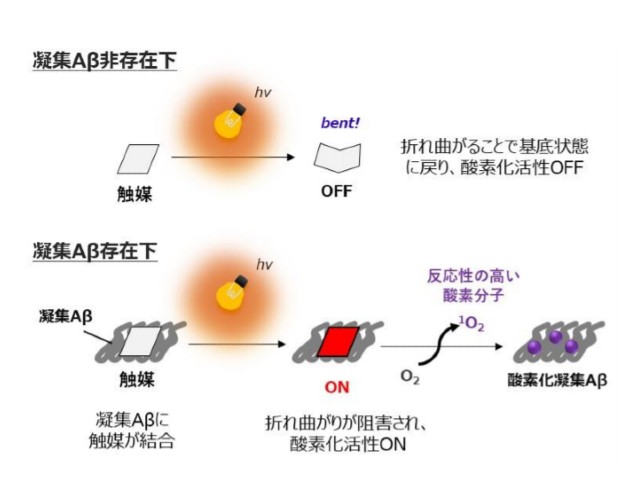
さらに,この触媒は,分子の屈曲運動性を活性発現のスイッチとすることにより,Aβを選択的に酸素化できる。すなわち,Aβが存在しない時は屈曲運動により触媒活性がオフになっており,Aβと結合すると運動性が低下して触媒活性がオンになる。このスイッチ機構は,副作用を抑えてAβに対し選択的に反応するために重要となる。
今回開発した触媒を静脈内投与したのち,体外から光を照射するという非侵襲的な手法により,アルツハイマー病モデルマウス脳内のAβを酸素化し,結果的に脳内のAβ凝集体を減少することに成功したという。
研究グループは今後,マウス脳内でのAβの酸素化により脳の機能が回復するか,アルツハイマー病に見られる行動異常などの症状が改善するか,などについて検討を進める。同時に,マウスと比べて頭蓋骨の厚いヒトにおいても非侵襲的な脳内Aβの酸素化が可能かどうかなど,臨床応用に則した観点での検討を進めていく。
現在,アルツハイマー病に対する根本的治療薬は存在しないが,この成果は,アルツハイマー病治療法の創出につながることが期待されるもの。また,このような触媒反応を用いた触媒医療戦略は,同じくペプチドやタンパク質が凝集して発症する様々な疾患(アルツハイマー病以外の認知症,パーキンソン病,筋萎縮性側索硬化症,末梢アミロイドーシスなど)に対しても,普遍的に適用できる概念だとしている。