 豊橋技術科学大学は,酸化チタンナノチューブ(Titanium oxide Nanotube:TNT)を用い,ナノ秒パルスレーザー照射による高効率な細胞内デリバリ法を開発した(ニュースリリース)。
豊橋技術科学大学は,酸化チタンナノチューブ(Titanium oxide Nanotube:TNT)を用い,ナノ秒パルスレーザー照射による高効率な細胞内デリバリ法を開発した(ニュースリリース)。
細胞医療や再生医療のためには,細胞の生存率とトランスフェクション(人為的に核酸を導入する)能力が高く,生きている細胞に外部分子をデリバリする手法が重要で,ウイルス法,物理的手法,化学的手法に分類される。
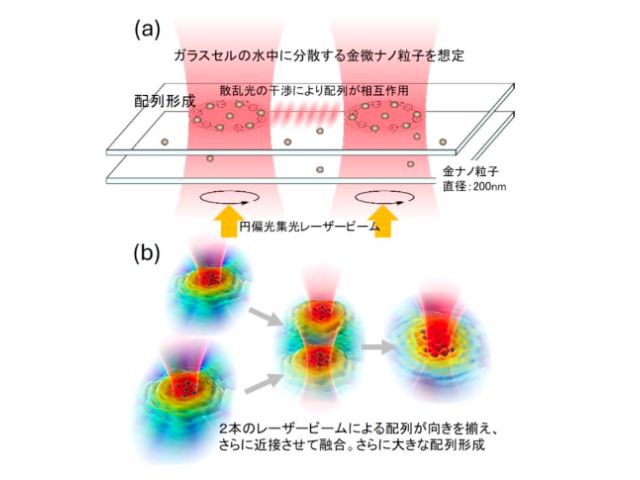
この内,パルス光照射による細胞内デリバリは,細胞への侵襲性が低く,新しい手法として注目されている。ここでは細胞を穿孔するために,パルス光を吸収させる金ナノ粒子などを溶液中に分散して利用されるが,材料が高価なため,よりコストを低減したナノ材料が望まれていた。
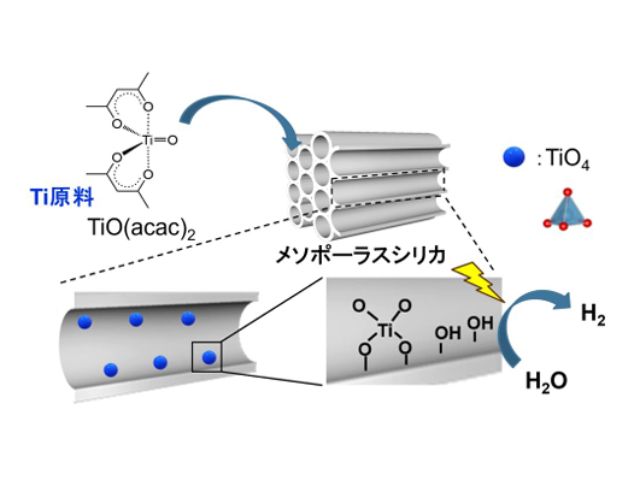
研究グループでは,光照射に基づく細胞内デリバリのための費用対効果の高いナノチューブアレイを設計し,作製した。異なる電圧と時間において,電気化学的陽極酸化技術を用い,チタンシート上にTNTを形成した。
X線光電子分光法(XPS)での計測により,異なる陽極酸化電圧と時間で形成されたTNTには,微量のTi金属(Ti0)とともに,濃度の異なるTiO2,TixOy(TiO/Ti2O3/Ti3O5)のような異なるチタン酸化物種が存在した。
酸素欠陥の形成により,ナノチューブは半金属および金属的特性を有する。このような性質を持つナノチューブは,ナノ秒パルスレーザーを照射した後,様々なメカニズムで細胞内へのデリバリを促進する可能性があるという。
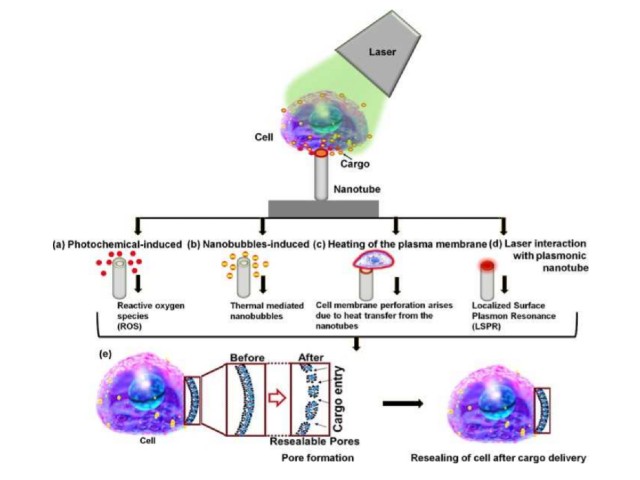
形成したTNT上に細胞を培養した後,生体分子溶液を導入し,532nmのナノ秒パルスレーザーを照射したところ,ヨウ化プロピジウム(PI)とデキストランをHeLa細胞(HeLa,ヒト子宮頸がん細胞)に高いトランスフェクション効率と細胞生存率で導入することに成功した。
細胞膜穿孔の原理としては,熱を介したナノバブル,光化学的に誘起される活性酸素種(ROS),ナノチューブから細胞膜への熱伝達,局所的な表面プラズモン共鳴高電磁場増強の各ナノチューブ上での形成,といった可能性があるという。
これにより,細胞膜-ナノチューブ界面にキャビテーション性ナノバブルが形成され,急速に成長,合体,崩壊して爆発を起こし,細胞膜穿孔を引き起こし,生体分子を細胞外から細胞内に送り出したと考えられる。
低コストに作製できる酸化チタンナノチューブは,高効率と細胞生存率を備え,並列で制御された均一なデリバリであるため,細胞治療や再生医療への応用が期待できるといている。