 早稲田大学と近畿大学の研究グループは,軸性キラリティを有する炭素,水素のみからなる多環式芳香族炭化水素(polycyclic aromatic hydrocarbons:PAHs)の高エナンチオ選択的合成に成功した。さらに,合成された分子は優れた発光特性を有することを明らかした(ニュースリリース)。
早稲田大学と近畿大学の研究グループは,軸性キラリティを有する炭素,水素のみからなる多環式芳香族炭化水素(polycyclic aromatic hydrocarbons:PAHs)の高エナンチオ選択的合成に成功した。さらに,合成された分子は優れた発光特性を有することを明らかした(ニュースリリース)。
近年,PAHsは有機電子材料へ応用されるなど,次世代の有機分子として精力的に研究が行なわれている。特にキラルなPAHsは特異な光学特性である円偏光発光(CPL)特性を有する場合があり,次世代の3Dディスプレーなどへの応用が期待されている。
効率的にキラルなPAHsを得るための合成方法として,キラルな触媒を用いて,触媒的にキラルPAHsを得る手法が開発されている。しかしながら,その手法はらせん構造に由来するキラリティを持つPAHsにのみ限られており,軸性キラリティを有するPAHsのエナンチオ選択的合成の報告はなかった。
今回,研究グループは,2つのベンゼン環からなるビフェニレンとアルキン部位が連結した化合物から,キラル遷移金属触媒を用いて軸性キラリティを有するPAHsのエナンチオ選択的合成に挑んだ。
今回用いたビフェニレンは,中央の四員環部分に大きな歪みを有しており,遷移金属触媒によって容易にその炭素―炭素結合を切断できる。しかしながら,置換基を持つビフェニレンの場合,置換基のない空いた炭素―炭素結合が選択的に切断を受ける。
そこで置換基部位に金属と相互作用するアルキン部位を導入することで,目的の炭素―炭素結合を選択的に切断する手法を開発した。アルキン部位は金属を目的の場所に接近させる「配向基」の役割だけでなく,金属触媒と反応し新たな芳香族化合物へ変換するための「反応部位」としての役割もある。
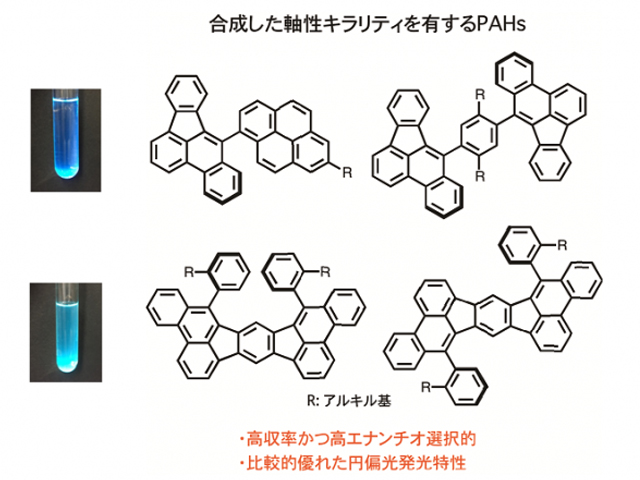
それにより,4つのベンゼン環で構築されるベンゾフルオランテン誘導体を得ることに成功した。またアルキン部位に置換基を持つベンゼン環を導入し,その置換基とベンゾフルオランテン骨格との立体反発により,軸性キラリティを構築した。
キラルロジウム触媒を用いる反応により,非常に高いエナンチオ選択性かつ非常に高い収率で軸性キラリティを有するPAHsの合成に成功した。さらに反応部位を2つ有する化合物を用いることで7つのベンゼン環からなるキラルPAHsの効率合成も達成した。また,得られたPAHの一つは,小分子として比較的優れたCPL特性を有していることを明らかにした。
今回得られた分子は比較的優れた光学特性を有していたことから,CPL特性を活用した技術(3Dディスプレー,セキュリティーペイント等)への応用が期待されるとしている。