九州大学,東京医科歯科大学,東京大学,群馬大学の研究グループは,水中で近赤外光から青色光へTTA-UCを示すヒドロゲル(ほとんど水からなる成型可能な高分子材料)の開発に初めて成功し,さらに発生した青色光をオプトジェネティクスに応用することで,神経細胞の形態を制御することにも成功した(ニュースリリース)。
フォトン・アップコンバージョン(UC)は,エネルギー分野(光触媒,太陽電池)やバイオ分野(光線力学療法,オプトジェネティクス)が直面している波長の制約を克服できると考えられ,世界中で活発な研究が行なわれている。
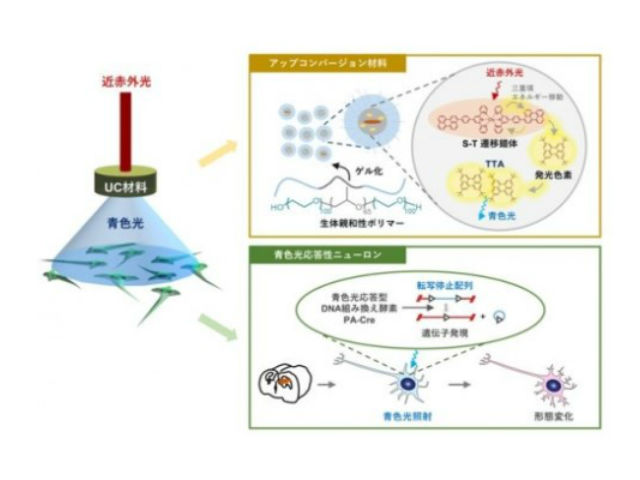
特に,三重項-三重項消滅(TTA)と呼ばれる分子間の三重項エネルギー移動に基づくTTA-UC機構は,比較的弱い光でも駆動しうるため生体を傷つけずに遺伝子操作できるという利点があるが,これまで水中において近赤外光を青色光に変換するための有効な方法論がなかった。
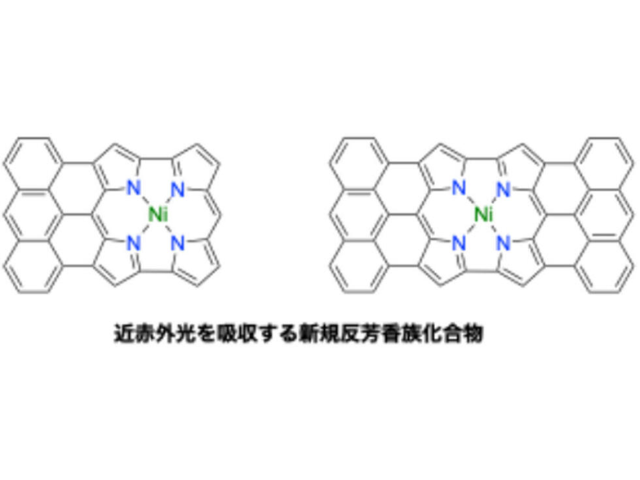
研究グループは近年,基底一重項状態から励起三重項状態への直接遷移(S-T吸収)を示す金属錯体を三重項増感剤(ドナー分子)として用いることで,バイオ分野への応用に必要な近赤外-青TTA-UCを可能にした。
しかし,三重項増感剤の励起状態の寿命が短いため,ヒドロゲルのような粘度が高く分子拡散が抑制される環境では三重項エネルギーを発光色素(アクセプター分子)に受け渡す前に失活してしまい,TTA-UCを起こすことは困難だった。
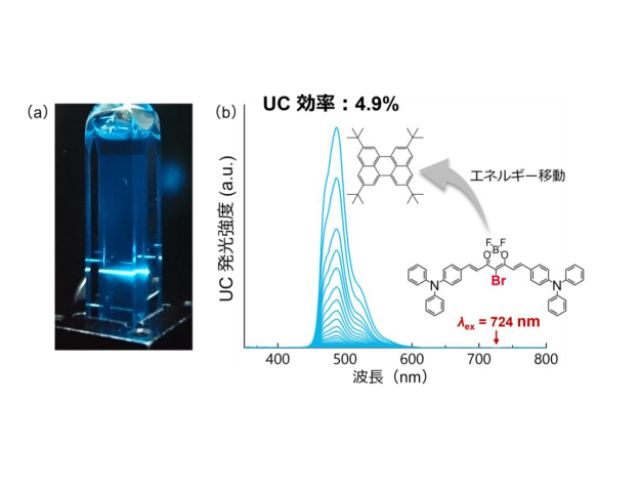
そこで今回の研究では,S-T吸収を示すドナー分子にアクセプター分子を連結させ,より励起寿命の長いアクセプター部位に励起エネルギーを溜めることにより,従来より120倍も長寿命な三重項励起状態を達成した。これにより粘度の高いヒドロゲル中においても三重項エネルギーを発光色素に受け渡し,アップコンバージョンできることがわかった。
また,TTA-UCに必要な三重項励起状態は通常水中に溶存する酸素により容易に失活してしまうが,加熱処理によりゲルを構成するミセルの集合状態を変化させて酸素の侵入を阻害することにより,空気中においてもTTA-UC発光を示すヒドロゲルの開発に成功した。
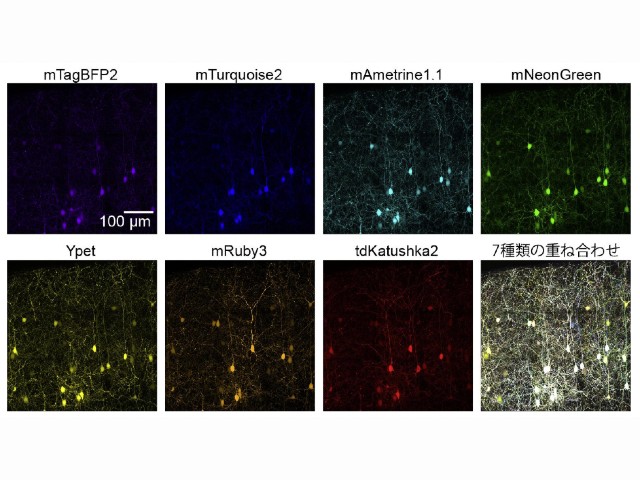
青色光に応答して細胞の形を操作できる遺伝子を神経細胞に導入し,その神経細胞を播種したシャーレにUC材料を浸漬して波長724nmの近赤外光を照射したところ,発生した青色UC発光により神経細胞の形態を制御できることが確認できたという。
研究グループは,今回開発したアップコンバージョン分子技術を発展させ,生体(ネズミやサルなどの動物個体)脳深部の神経細胞を遺伝子操作することによって,高次脳機能の解明が期待できるとしている。