東邦大学は,新しく開発したセンサータンパク質を使って,ネクロプトーシスと呼ばれる細胞死の様子をイメージングする技術を世界で初めて開発した(ニュースリリース)。
ネクロプトーシスはアポトーシスと同様に制御された細胞死だが,アポトーシスとは異なり細胞膜が早期に破裂することから死細胞の周囲に強い炎症を誘導することが知られていた。ネクロプトーシスは最近の研究から心筋梗塞や脳梗塞などの虚血性疾患の悪化に寄与することが明らかにされている。
アポトーシスは,カスパーゼと呼ばれるプロテアーゼの活性化により引き起こされ,細胞膜は保たれるために周囲に強い炎症を引き起こすことは少ない。
これらの細胞死の進行を生きた培養細胞の細胞内で可視化(細胞を殺したり破壊したりせずに,顕微鏡で実際に細胞死が進行しているかを観察)する技術の開発は,細胞死がどのような状況で起こっているのか,またその結果としてどのような反応を周囲の細胞に誘導するのかを解析する上で非常に重要。
これまでにアポトーシスについては,細胞死の進行時にカスパーゼと呼ばれる酵素が活性化することを利用して,FRETと呼ばれる2つの蛍光分子がごく近接して存在する場合に,1つの蛍光分子からもう1つの蛍光分子へとエネルギーが移動する技術を用いて可視化することが報告されていた。
しかし,ネクロプトーシスの場合には,カスパーゼのようなタンパク質分解酵素が活性化しないために,同様の方法でイメージングすることは不可能であり,可視化における大きな障壁となっていた。
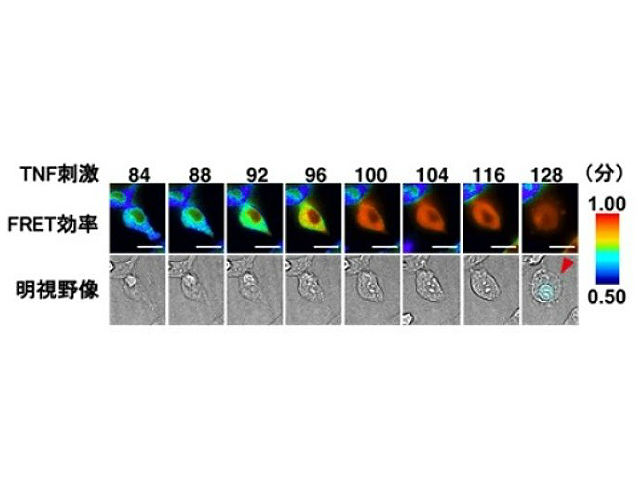
今回研究グループは,MLKLと呼ばれるネクロプトーシスの実行因子がネクロプトーシス誘導細胞では立体構造が変化する事に注目して,FRETの原理を利用したセンサータンパク質「SMART」を作成し,世界で初めてネクロプトーシスの様子を蛍光イメージングする事に成功した。
さらに研究グループは,1細胞分泌実時間イメージング法という最新の技術を用いることで,細胞死に伴って放出され,さまざまな病態に関与する細胞内物質「DAMPs」のネクロプトーシス細胞からの放出には遷延モードと破裂モードの2種類があることを見出した。
研究グループは今後,ネクロプトーシスおよびネクロプトーシスに伴い放出されるDAMPsが関与する病態の解明や,治療技術の開発が加速することが期待されるとしている。