 東京大学と東邦大学は,可視光照射下で二種類の触媒を組み合わせることにより,光反応で生じたアルキルラジカルをプロパルギル位でエナンチオ選択的に補足することで,プロパルギル位に単純なアルキル基をエナンチオ選択的に導入することに世界で初めて成功した(ニュースリリース)。
東京大学と東邦大学は,可視光照射下で二種類の触媒を組み合わせることにより,光反応で生じたアルキルラジカルをプロパルギル位でエナンチオ選択的に補足することで,プロパルギル位に単純なアルキル基をエナンチオ選択的に導入することに世界で初めて成功した(ニュースリリース)。
プロパルギル位に不斉炭素を有するプロパルギル位置換化合物は,医薬品として極めて重要な化合物群となっている。プロパルギル位に直接置換基をエナンチオ選択的に導入する触媒的不斉プロパルギル位置換反応に関しては,2000年以降,東京大学の研究グループなどにより,積極的に開発が進められてきた。
しかしながら,単純なアルキル基を導入する触媒的不斉プロパルギル位アルキル化反応については,アルキル化求核剤の反応性が高すぎるため,これまで報告例がなかった。
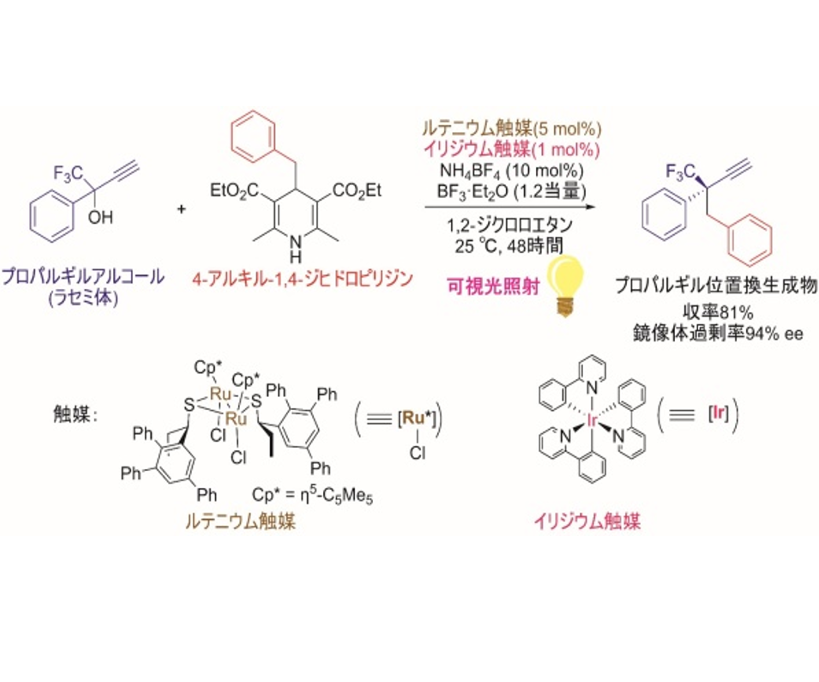
今回,研究グループは,イリジウム触媒の存在下,可視光照射による光反応でアルキルラジカルを生成する4-アルキル-1,4-ジヒドロピリジン(4-アルキル置換ハンチュエステル)に着目し,これを求核的なラジカル反応剤として用いることで,プロパルギルアルコールのエナンチオ選択的な触媒的プロパルギル位アルキル化反応に世界で初めて成功した。
この触媒反応は,イリジウム触媒による光レドックス反応と,ルテニウム触媒による不斉プロパルギル位置換反応という,二種類の触媒反応系を組み合わせることで実現した。
すなわち光反応によって4-アルキル-1,4-ジヒドロピリジンから生じたアルキルラジカルを,プロパルギル位置換反応における重要な反応中間体であるアレニリデン錯体が適切に補足することにより,目的の生成物が得られており,ルテニウム触媒がラジカル反応や単一電子移動で生成する反応中間体を安定化する鍵として働いたことを示す。
こうして,光反応で生成したフリーラジカルをマイルドなアルキル化剤として利用することで,これまでイオン性の求核剤では実現できなかった,プロパルギル位への単純なアルキル基のエナンチオ選択的な導入に世界で初めて成功し,さらにプロパルギル位における全炭素不斉四級炭素の構築にも成功した。
この反応系は,可視光照射下、常温で反応が進行しており,従来の反応系に比べて反応条件はよりマイルドであり,さらに従来の反応系で必要であった化学量論量の有機金属アルキル化剤やハロゲン試薬などを必要とせず,研究グループは,従来の反応系に比べてより環境に優しいクリーンな反応系だとしている。