 東京大学大,基礎生物学研究所,山口大学,北里大学は,アメーバや免疫細胞などのはいまわる細胞の形を,深層学習によって特徴づけ,その動きを特徴づけるダイナミクスのモデル解析を通じて,その基本制御機構の新たな数理的描像を得ることに成功した(ニュースリリース)。
東京大学大,基礎生物学研究所,山口大学,北里大学は,アメーバや免疫細胞などのはいまわる細胞の形を,深層学習によって特徴づけ,その動きを特徴づけるダイナミクスのモデル解析を通じて,その基本制御機構の新たな数理的描像を得ることに成功した(ニュースリリース)。
動く細胞の形とそのダイナミクスを数理的に表現することは,多細胞組織中の運動特性や情報処理特性,細胞型やその病変の検出,予測にとって重要だが,数理シミュレーションで得られた形やその動きが、実際の細胞のそれをどの程度うまく表現できているのか,客観的検証はほとんどされていない。
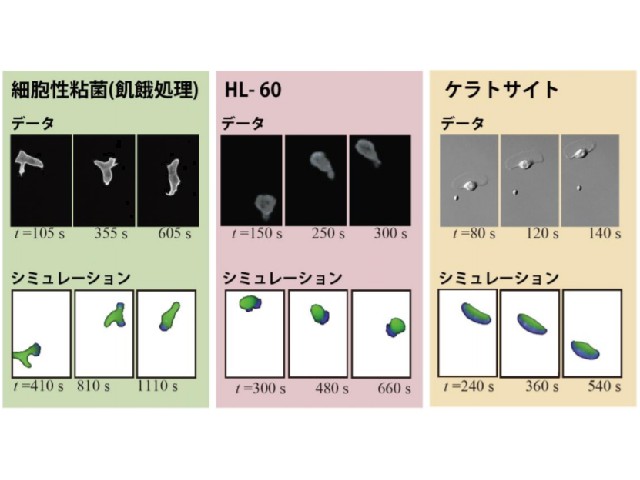
動く細胞がとる形は一見すると無秩序に見えるが,移動する方向にとってつぶれた餃子のようなもの,逆三角のもの,仮足を複数だした複雑なものが,種や細胞型を越えて典型として頻繁にみられる。
そこで,研究所グループは,この3つの典型的な形を示す細胞画像データを用い,画像認識に用いられる畳み込みニューラルネットワーク(CNN)によって,これら典型の分類器を構成し,この分類器を特徴づける出力チャンネルから,細胞の伸びている方向と形状の複雑さを表現する特徴量空間を得ることに成功した。
この手法は,事前知識によって多数の特徴量を決めておかずにすむのが大きな利点。得られた特徴量空間で,実際の細胞とこれまで提案されている代表的な数理モデルを比較検証したところ,いずれもアメーバ状の形状特徴を十分に表現できていないことがわかった。
そこで,微小なゆらぎを増幅し一過的な仮足を形成する興奮系のダイナミクスと,保存量を含む双安定性によって極性を形成する機構を数理的に表現する,「理想細胞モデル」(ideal cell model)を新たに提案した。
体系的なパラメータ探索の結果をデータプールとして用意し,上記の特徴量空間において,参照点となる実際の細胞データと距離がもっとも近いものを選ぶと,その瞬間瞬間の形が似ているということだけでなく,モデルから予想されるダイナミクスも極めて実際の細胞に近いものが得られることが示された。
さらに,薬剤処理や遺伝子変異によって得られる異常な変形ダイナミクスについても,これらの形態異常の出現とモデルパラメータの変化とを結びつけることができた。これらの解析結果は,単一の数理モデルによって多様な形状ダイナミクスが統一的に記述されていることを示すという。
今回の成果は,生命科学とAI・画像解析技術との密接な連携を通じて,細胞運動機構の理解を大きく進展させるもの。医学応用に向けた基礎としても期待されるとしている。