 名古屋大学と抗体技術のペルセウスプロテオミクスは,GPR87を分子標的とする抗ヒトGPR87モノクロナール抗体を開発し,その抗体を用いた悪性中皮腫,肺癌に対する近赤外光線免疫療法の応用開発に成功した(ニュースリリース)。
名古屋大学と抗体技術のペルセウスプロテオミクスは,GPR87を分子標的とする抗ヒトGPR87モノクロナール抗体を開発し,その抗体を用いた悪性中皮腫,肺癌に対する近赤外光線免疫療法の応用開発に成功した(ニュースリリース)。
世界の癌死の中でも肺癌は最も多い。また,悪性胸膜中皮腫は近年増加傾向であり,治療法が限られるうえ,予後が非常に悪いため,いずれの疾患も新たな治療法が求められている。
GPR87というタンパク質は成人の正常細胞には発現は乏しく,肺癌,膵臓癌,子宮頚癌,皮膚癌などの様々な癌細胞の細胞膜に発現していることが確認されており,癌治療の有力な治療標的と考えられている。しかし,その生理的機能など不明な点が多く治療薬の開発は進んでいない。
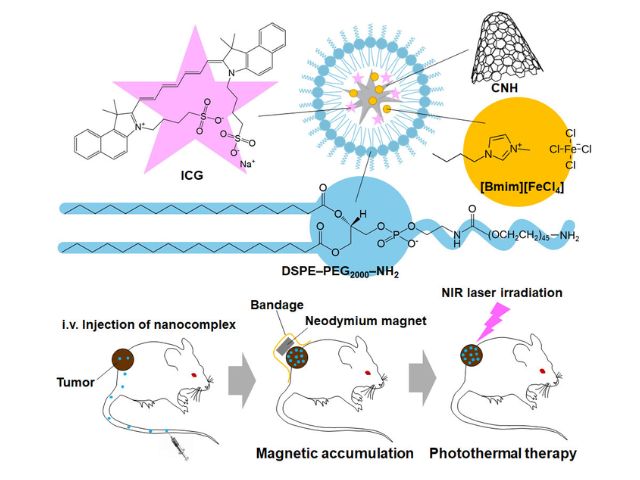
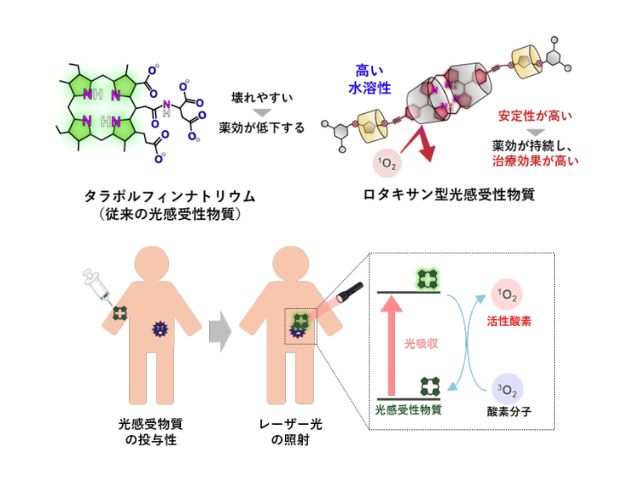
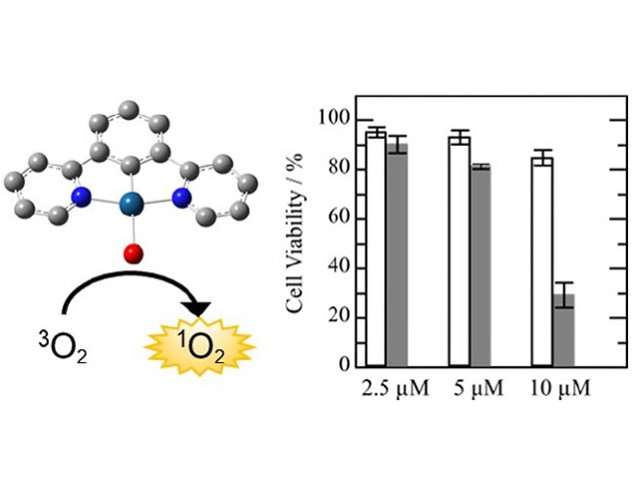
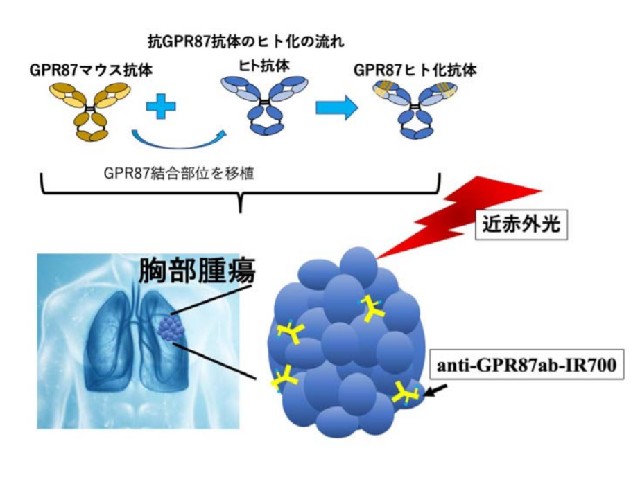
近赤外光線免疫療法は,癌細胞が発現するタンパク質を特異的に認識する抗体と光感受物質IR700の複合体を合成し,その複合体が細胞表面の標的タンパク質に結合している状態で690nm付近の近赤外光を照射すると細胞を破壊する。研究グループはGPR87を標的とした近赤外光線免疫療法の開発を行なった。
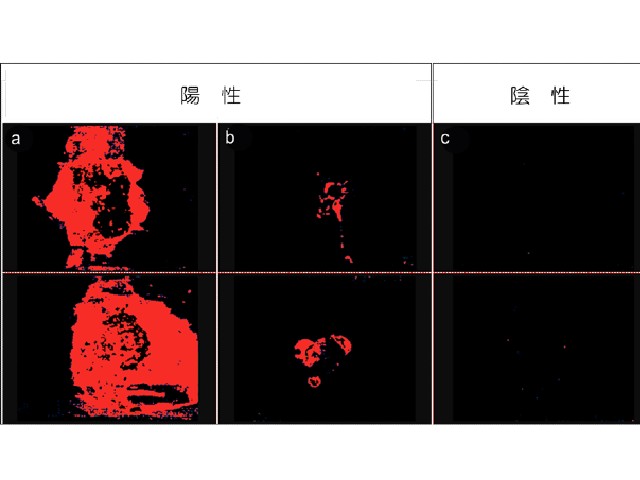
研究グループが手術検体を用いて腫瘍組織に免疫染色を行なった結果,非小細胞肺癌の約6割,小細胞肺癌の4割,悪性胸膜中皮腫は全例でGPR87の発現を認めた。
抗GPR87ヒト化抗体(GPR87ab)を開発し,抗GPR87抗体(GPR87ab)と光感受物質 IR700 の複合体を合成してGPR87ab-IR700を作成。これを用いて,肺癌・悪性胸膜中皮腫細胞に対する近赤外光線免疫療法を実施した。
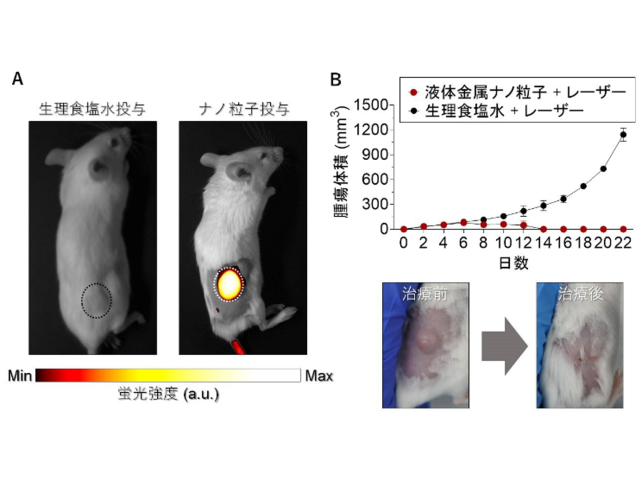
顕微鏡で観察したところ,近赤外光の照射後,速やかに細胞の膨張,破裂,細胞死が見られたという。標的細胞と非標的細胞に同時に近赤外光を照射したところ,標的細胞のみに細胞死が起こり,非標的細胞には特に影響はなかった。マウスの担癌モデルにおいては有意な腫瘍の増大抑制と生存の延長が示された。
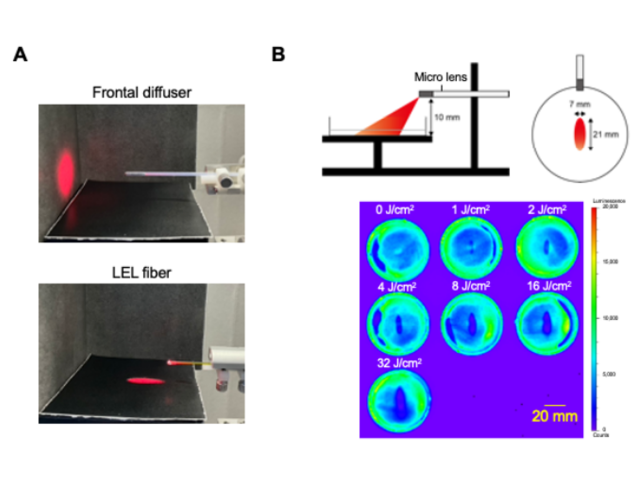
この成果は,近赤外光線免疫療法を人の肺癌治療,悪性胸膜中皮腫へ応用する際,基礎的知見として貢献することが期待されるとする。また,今後,胸部腫瘍に対する近赤外光の照射デバイスの開発や従来の治療との併用など,更なる応用が検討されているとしている。