 東京工業大学は,細胞内のpH変化をリアルタイムにモニターできる新しい発光型タンパク質センサーを開発し,光合成反応に伴って細胞内のpHが変化する様子を捉えることに成功した(ニュースリリース)。
東京工業大学は,細胞内のpH変化をリアルタイムにモニターできる新しい発光型タンパク質センサーを開発し,光合成反応に伴って細胞内のpHが変化する様子を捉えることに成功した(ニュースリリース)。
細胞内の様々な生理状態の変化を探るために,これまで緑色蛍光タンパク質GFPをベースとするタンパク質センサーが数多く開発されてきたが,これらを光合成生物で用いる場合には,測定に必要な励起光が光合成反応に影響してしまう点が大きな問題だった。
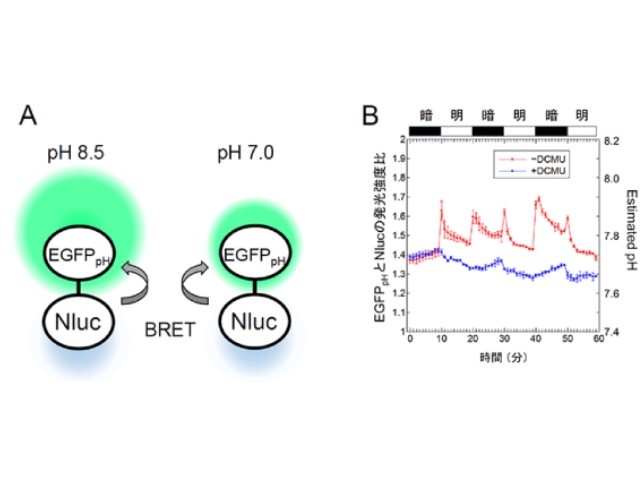
研究では,GFPに様々な変異を導入し,pH7~8.5の範囲でpHの変化に応じて蛍光強度が直線的に変化するセンサータンパク質EGFPpHを作成した。このEGFPpHを励起光源ではなく生物発光によって励起するために,市販の発光タンパク質NanoLucを励起光源タンパク質として採用した。
NanoLucは,海生のトゲオキヒオドシエビ由来のルシフェラーゼを商品化したもので,Furimazineという化合物を添加することで460nmを発光スペクトルのピークとする極めて強い光を発する。
NanoLucとEGFPpHを結合すると生物発光共鳴エネルギー移動(BRET)が起こり,EGFPpHの蛍光がpHに応じて510nm付近をピークとして観察された。研究グループは,この励起光を必要としない新たな発光型センサータンパク質を「Luphin」と命名した。Luphinは細胞内で発現した場所のpH,あるいはその変化を自在に測定できる。
光合成反応では,光合成電子伝達反応によってNADPHが生成されるとともに,チラコイド膜という閉じた膜系の内側に水素イオンが輸送され,酸性の状態にする。Luphinを用いることで,このような細胞内の水素イオンの移動をリアルタイムに捉えられることが確かめられたという。
さらに,水素イオンの移動が,予想されていた光照射時だけでなく,明条件から暗条件に移したときにも起こり,光合成細胞内の水素イオン動態が様々な因子によって制御されていることが明らかになった。
研究グループは今後,Luphinのシグナルを手がかりに,細胞内で働く様々な因子の働きが明らかにできるものと期待している。