 京都大学,理化学研究所,東京大学の研究グループは,マウスの体節が形成される際にみられる細胞間で同期した遺伝子発現量の振動を生じさせるためには,細胞間シグナル伝達時間の適切な遅れが重要な役割を果たすことを明らかにした(ニュースリリース)。
京都大学,理化学研究所,東京大学の研究グループは,マウスの体節が形成される際にみられる細胞間で同期した遺伝子発現量の振動を生じさせるためには,細胞間シグナル伝達時間の適切な遅れが重要な役割を果たすことを明らかにした(ニュースリリース)。
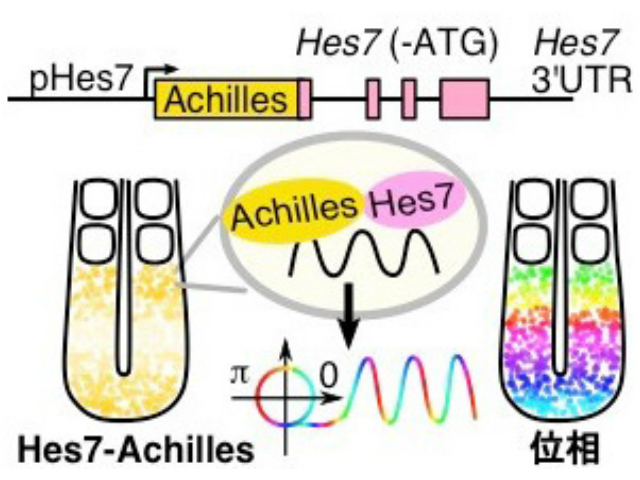
脊椎動物では,受精卵から体が形づくられる発生の過程で,背骨・肋骨などの「節目」構造の元となる,体節と呼ばれる組織が周期的に形成される。この体節形成の周期を制御するメカニズムは分節時計と呼ばれ,Hes7遺伝子の発現量がリズミカルに振動することがその中心的な役割を担っている。細胞内でのHes7遺伝子発現量の振動リズムが細胞間で同期することで,組織レベルのダイナミクスへつながる。
この組織レベルでのHes7遺伝子発現量の同期が,規則正しい体節形成に重要であると考えられている。しかし,これまで,マウス胚において1細胞レベルでHes7遺伝子の振動を観察することが困難であり,細胞どうしの同期が生じる際の分子的なメカニズムは明らかにされていなかった。
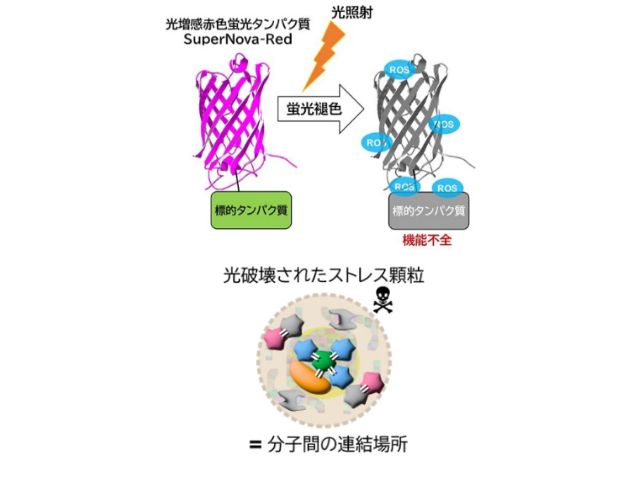
半減期が約20分程度と非常に短命なHes7タンパク質の動態を追うために,既存の黄色蛍光タンパク質を改良し,成熟速度を速めた新規の黄色蛍光タンパク質Achillesを開発した。研究では,Achillesを用いたマウス胚のライブイメージングにより,Hes7遺伝子の発現量を1細胞レベルで計測し,個々の細胞での振動の様子を可視化することに成功した。
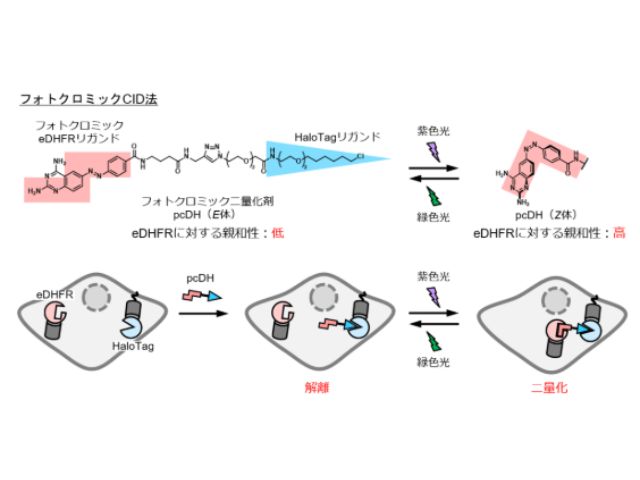
さらにこの系とオプトジェネティクスなどを用いて,糖転移酵素の1種であるLunatic fringe遺伝子が,細胞間のシグナルの伝達に適切な遅れを生み出し,これが同期を促進することを明らかにした。
この成果は,細胞間のシグナル伝達の時間の調節が集団レベルのダイナミクスに及ぼす影響について明らかにしたもの。Lunatic fringe遺伝子はヒトにおける先天性側弯症の原因遺伝子として知られており,こうした遺伝疾患の発生メカニズムや,ホタルの集団発光やメトロノームの同期現象などといった,自然界に普遍的にみられるリズム現象の同期メカニズムの理解につながるとしている。