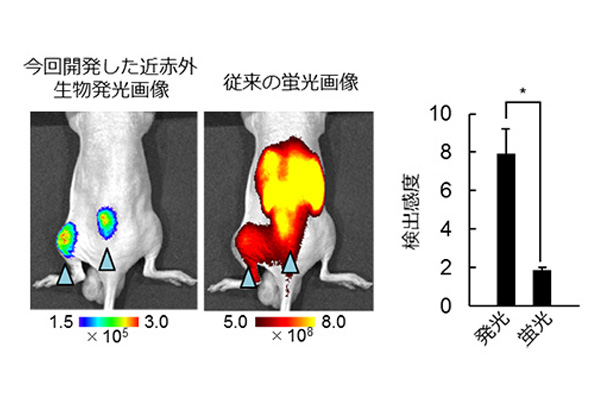
 東京工業大学は,腫瘍組織に存在する悪性化したがん細胞を非侵襲的に可視化することに成功した(ニュースリリース)。
東京工業大学は,腫瘍組織に存在する悪性化したがん細胞を非侵襲的に可視化することに成功した(ニュースリリース)。
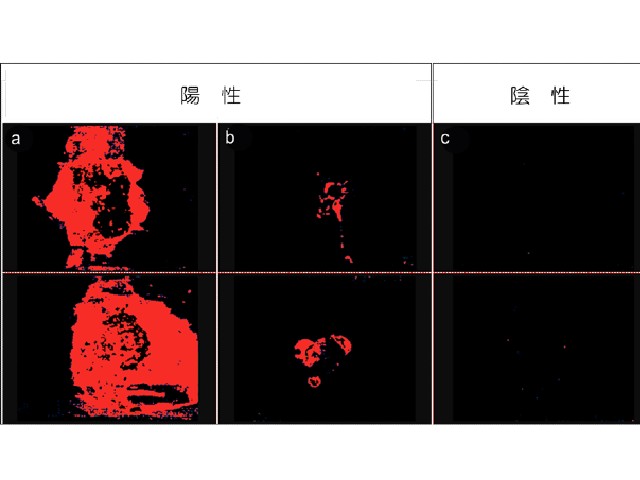
悪性がん細胞で活性化する低酸素誘導因子に応答して,近赤外発光を生成するイメージングプローブ(POL-N)を開発して実現した。このイメージングプローブはユビキチン-プロテアソーム系(UPS)による低酸素誘導因子の分解制御機構と,近赤外生物発光分子を組み合わせたタンパク質分子であり,血中に投与するだけで,高感度かつ迅速に腫瘍組織の低酸素誘導因子を発光できた。
低酸素誘導因子は多くの腫瘍組織で活性化が認められ,薬剤抵抗性や転移といった悪性化に関わることが報告されており,治療標的や診断マーカーとして有望。これまで,腫瘍組織における低酸素誘導因子の活性化を非侵襲的に可視化するためには,がん細胞やマウスに前もって遺伝子を導入する必要があり,その場観察は困難だった。
今回の研究では,これまでの蛍光イメージングプローブの欠点を解消するため,光シグナルの精密な制御が可能な生物発光タンパク質ウミシイタケルシフェラーゼ(Rluc)を利用した。しかし,Rlucが生成する最大発光波長は547nmと,生体組織に吸収されやすく,生体組織の非侵襲イメージングには不向きであった。
そこで,Rlucに近赤外蛍光色素を結合し,生物発光共鳴エネルギー移動(生物発光反応によって生成されたエネルギーが近傍の蛍光物質に移動する現象)を介して最大発光波長を702nmに長波長化することで,この問題を解決した。
開発したイメージングプローブは,外部から生体に血中投与した後,低酸素誘導因子が活性化したがん細胞内に蓄積され,生体組織透過性の高い近赤外発光シグナルを生成することで悪性化したがん細胞を可視化する。マウスを用いたがんの悪性化機構に関する研究を加速させるとともに,低酸素誘導因子が関わる多くの疾患研究に有用なツールとなるとしている。