
慶應義塾大学・客員教授の末松誠氏,同医学部医化学教室・専任講師の山本雄広氏らの研究グループは,富士フイルム・先端コア技術研究所・研究員の塩田芽実氏,同研究主幹の納谷昌之氏らとの共同研究で,表面増強ラマンイメージング(SERS imaging)を用いて,マウス凍結病理組織切片におけるがん部と非がん部の代謝プロファイリング解析を行ない,両者の違いを統計的に分析することによって,がんの所在を非標識・無染色で自動的に可視化することに成功した。
がんは遺伝子変異によって,自らの生存に有利な各種の代謝物を生成し,周囲の非がん組織と異なる代謝特性を示す。また活発に周囲の正常組織から自らの生存に必要な代謝物を収奪し増殖していることが,近年の研究で明らかにされてきた。そのような代謝物の中でもグルタチオンやシステイン,硫化水素などの硫黄を含む代謝物(含硫代謝物)は強力な抗酸化物質として,がん細胞の生存,増殖や薬剤耐性などに関与することが示唆されているが,実態は明らかではなかった。
一方,がんの病理診断は主として染色や抗体による標識を施した組織試料を病理の専門家が光学顕微鏡で調べることによって行なわれる。生化学的な自動補助診断技術の開発は,病理医の業務の負担軽減につながるだけでなく,抗がん剤に対する耐性の有無や悪性度の判定など,がんの患者さんに資する「質的診断」に役立つ可能性がある。そこで今回の共同研究では,がんに固有の多様でかつ多数の代謝物の分子情報を包括的に把握する方法としてSERS imagingを利用することを検討した。
SERS imagingは,金のナノ粒子をランダムに敷き詰めた特殊基板に近赤外レーザー光を照射することによって発生する近接場光(強力な電磁場の増強スポット)を利用し,基板上の生体試料に含まれる各種の代謝物の原子間振動を反映するラマン散乱光を増強して,代謝物の2次元画像として検出する技術。
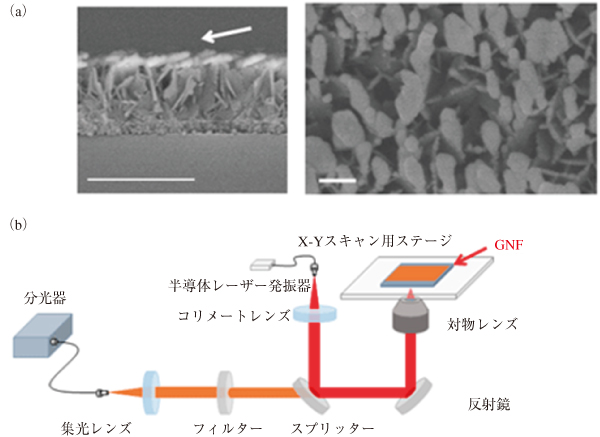
(a)の矢印は金を蒸着させた方向を示す。白く光っている部分が「そらまめ状」の金ナノ粒子であり,それを上から見た写真が右になる。(a)のバーは左が500 nm,右が100 nm。
研究では,富士フイルムが金ナノ粒子の自己組織化を利用し,世界に先駆けて開発したSERS基板(図1)を用い,数センチ角の病理組織中の代謝物について,発生するラマン散乱光を高感度・高解像度で画像化する技術を確立した。
この技術を用い,ヒト大腸がん細胞株を免疫不全マウスの脾臓に移植してできる異種移植肝転移モデルと,共同研究者である慶應義塾大学・医学部先端医化学研究所・教授の佐谷秀行氏らが開発した,Ink4a/Arfノックアウトマウス由来の神経幹細胞にH-RasV12遺伝子を導入後に移植して発生する同種神経膠芽腫モデルの,2つの実験モデルで得られるラマン散乱光のスペクトル上にあるピーク(SERS信号)を,がん部,非がん部で詳細に分析した。これらのモデルのがん組織は,実際のヒトの悪性腫瘍と同様の複雑な様相となっている。
異種移植大腸がんモデルのがん部を含む組織切片のSERS imagingを隣合った切片の質量分析イメージングのデータと照合することにより298 cm–1のSERS信号がシステインから生成される還元型グルタチオン(GS)を,978 cm–1が同じくシステインから生成されるヒポタウリン(HT)を反映するSERS信号であることを特定した(図2)。
画像上で行なったがんの診断所見と照らし合わせた結果,大腸がん肝転移モデルではがん部にグルタチオンが豊富に検出できる一方,ヒポタウリンはむしろがんの外側の肝臓実質に存在することが分かったという。
この結果から,多数の代謝物から検出される原子間振動の,がん部と非がん部の特徴の違いに基づき,がんの所在を検出できる可能性が示された。
そこで研究グループは,複数の代謝物のSERS信号をがん部,非がん部で区別して統計的に分析し,それぞれの部位に特異的なSERS信号を多数抽出した。さらに,これらの特異的な信号をバイオマーカー・シグニチャーとして利用し,これを病理医によるがん部,非がん部の診断結果のセットと共に「教師データ」としてSERS imagingを解析する画像処理技術を開発した。

病理医がヘマトキシリン・エオジン染色像(H-E上段左)で検鏡して得られた「教師データ」で描出したがん部(上段中央)の画像情報に基づき,がん部,非がん部に特異的なSERSシグナルを統計的に抽出し,がん部の自動抽出を行なった(上段右)。がん部に顕著に認められる代謝物として活性硫黄種であるポリスルフィドとヒポキサンチン,イノシン1リン酸(IMP)などに含まれるアデニン環含有代謝物が同定された。ポリスルフィドは強力なレーザーを用いる質量分析では分解するため検出できなかった。(バーは上段が2 mm,下段が0.5 mm。)
この技術は,がん部と非がん部の境界判定が難しい神経膠芽腫(グリオブラストーマ)モデルにおいても,未知の検体のどこにがんが存在するかを自動的に抽出することができるもの(図3)。また,このモデルのがん部で高いピークを示す化合物の同定を行なったところ,485 cm–1のSERS信号に対応する活性硫黄であるポリスルフィドと,726 cm–1のSERS信号に対応するヒポキサンチンやイノシン1リン酸(IMP)などのアデニン環含有代謝物が,神経膠芽腫のがん部に豊富に含まれることが明らかになったという。
この技術創出により,熟練した病理医が診断したがん部,非がん部におけるSERS信号を「教師データ」として収集することが可能になり,未知の凍結組織切片を用いて非標識・未染色で自動的にがん部を抽出することができる,自動診断支援システムへの展開の可能性が開かれたとしている。
SERS imaging技術は生体を構成する低分子化合物の全体像を捉えることのできる新しいメタボロミクス解析技術で,生化学的なアプローチによる補助診断技術となる可能性がある。
また,多数の検体を短時間かつ簡便に解析できるこの技術をがんの質的診断に応用することで,がんの術中迅速診断の自動化や境界領域の病変に対する補助診断として活用できる可能性もある。さらにこの技術は,がんの代謝プロファイリングデータに基づく化学療法や放射線療法などの治療法の最適化にも資する可能性もあることから,今後の展開が期待されている。◇
(月刊OPTRONICS 2018年6月号掲載)






























