■体内のプローブなどの位置を定量する
蛍光プローブなどを患部に入れることができても,生体組織は散乱や減衰が大きいため,体外から深さを含めたその位置を定量するのは難しく,光を用いた診断法の最大の課題となっている。
北海道大学助教の西村吾朗氏は,時間分解計測法によりこうしたバックグラウンドを区別し,目的の蛍光物質の存在を高感度で確認できるアルゴリズムを開発した。
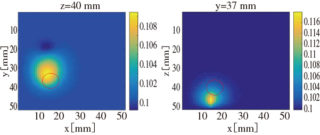
光源から体内に入った光子は,散乱によって様々なルートを通って検出器へと至るが,この時間をカウントすることで光路分布を求める。複数のチャンネルによる計測により,通常のカメラでは見ることができない深さにある蛍光体の検出と位置の同定が可能になる。
鶏肉を用いた模擬試料による実験では,ある程度の深さ同定に成功しているといい,今後は多チャンネル化やアルゴリズムの最適化が課題になるとしている。多チャンネル化に関しては,10 psオーダーでのフォトンカウンティングが必要なため,通信機器の技術が応用できるのではないかとしている。
■染色不要のイメージングシステム
生体分子や組織の観察に,試料へのダメージを考えて染色をしなくても観察が可能なラマンイメージングが行なわれている。最近では高速なイメージングが可能な誘導ラマン散乱顕微鏡法も注目されているが,この方法は多様な試料を観察するために光源のレーザーを広帯域で変調させる必要がある。しかし,波長可変レーザーの帯域幅と走査速度にはトレードオフの関係があり,また高速観察ために強いレーザーを入れると試料へのダメージの問題もあった。
大阪大学准教授の橋本守氏と静岡大学教授の川人祥二氏は,これらの問題を解決する多焦点誘導ラマン散乱イメージングシステムを開発している。このシステムは光源のレーザー部分を橋本氏が,検出器のカメラを川人氏が担当した。
今回両氏は,光源に高速(秒オーダー)で波長走査(100 nm程度)ができるピコ秒レーザーと,複数ビームによって励起光強度を低減し,かつ励起光強度が等しいシステムを開発するとともに,誘導ラマンを検出できるカメラを開発した。
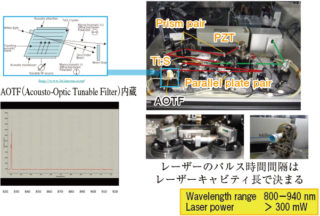
波長可変レーザーにはメガオプトの音響光学波長可変フィルター(AOTF)を用いたパルスレーザーを用いて広帯域での高速波長変換を実現した。ただし,このレーザーのパルス間隔はレーザーのキャビティ長で決まるため,試料にレーザーが同じタイミングで照射されるよう,光路上の2枚の並行平板をガルバノモーターで操作することで共振器長を変化させる技術を開発した。また,レーザーを同期させるために光学的にfsオーダーでパルスを同期させることにも成功した。
一方,カメラはポンプ光に対して105分1程度と極めて微弱な誘導ラマン散乱を捉える必要がある。そこで,各ピクセルにロックイン検出機能を設けてアレイ状に配列したセンサーの開発を行なった。現在は1ピクセルに着目したイメージングを実施しており,複数ピクセルについても同時動作の確認をはじめ,試作も完了しているという。
これらの技術はトータルではもちろん,個々の技術についても様々な応用が考えられるとして,研究グループでは企業からの協力・提案を待っている。◇
(月刊OPTRONICS 2016年10月号掲載)