横浜市立大学と北海道大学は,光線力学療法用光増感剤として両親媒性白金錯体を新たに開発し,ヒト臍帯静脈上皮細胞に対する選択的光細胞毒性や細胞内動態を明らかにした(ニュースリリース)。
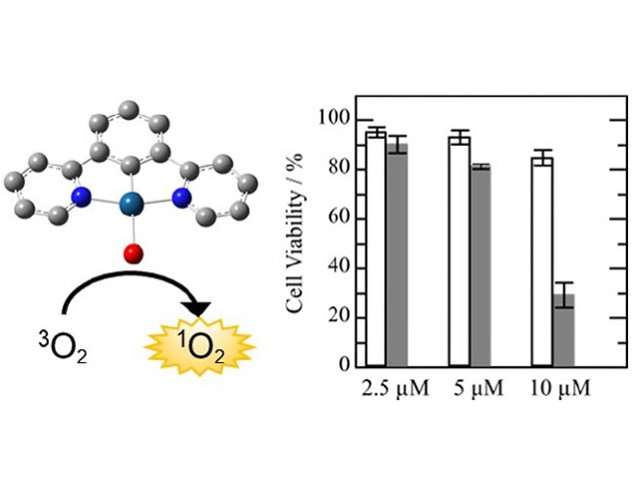
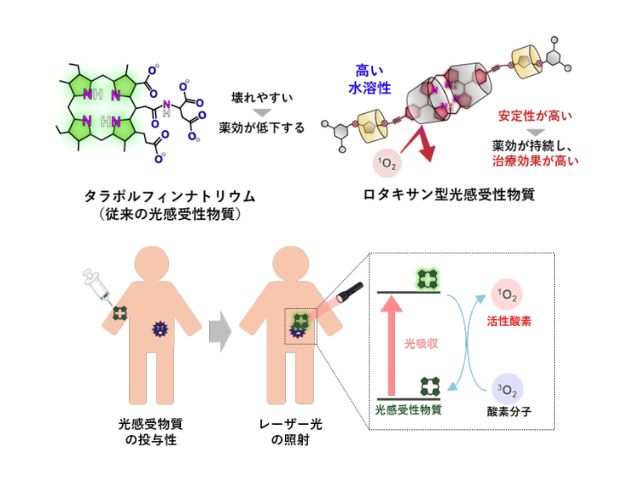
光線力学療法(PDT)は,光照射によって腫瘍組織を選択的に死滅させることができる非侵襲性のがん治療法の一つ。PDT用光増感剤としては,光誘起電子移動反応によってスーパーオキシドアニオンラジカル(O2·-)を生成させるType Iと,光誘起エネルギー移動反応によって一重項酸素(1O2)を生成させるTypeⅡがある。
白金錯体は重原子効果により励起三重項状態を効率よく生成することができるため,TypeⅡの光増感剤としてこれまで注目されてきた。
水に不溶な中性白金錯体を生体へ応用するためには,細胞への取り込みを改善するために両親媒性を得ることが重要になる。これまで,エチレングリコール基やペプチド基の導入した両親媒性の白金錯体が複数報告されてきたが,これらは多段階の化学合成を必要とするため,より簡便な方法での両親媒性の獲得が望まれていた。
研究では,白金錯体のイオン化,タンパク質内包による両親媒性の獲得に注目し,それらの合成,光物性解明,光細胞毒性試験を行なった。イオン化型白金錯体の一重項酸素生成量子収率は55%と高い値を示したのに対し,タンパク質内包型白金錯体は13%であることが分かった。
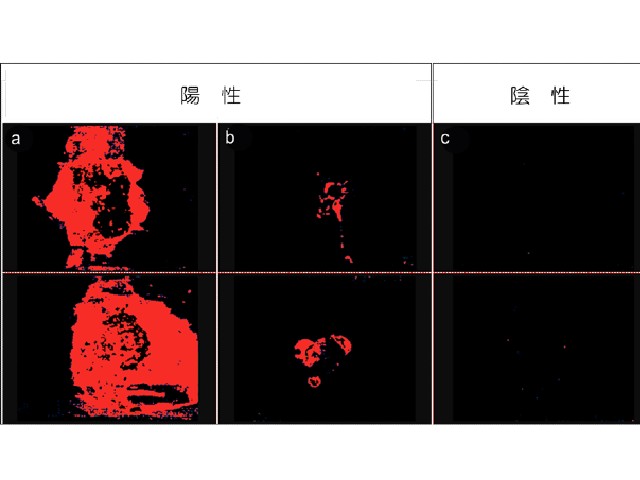
白金錯体で処理したヒト臍帯静脈内皮細胞(HUVEC)では,イオン化型白金錯体は拡散による急速な取り込み後に細胞全体に非局在化した一方,タンパク質内包型白金錯体はエンドサイトーシスによって取り込まれ,細胞小器官と細胞膜に局在化することが示唆され,細胞動態が二つで異なることが明らかとなった。
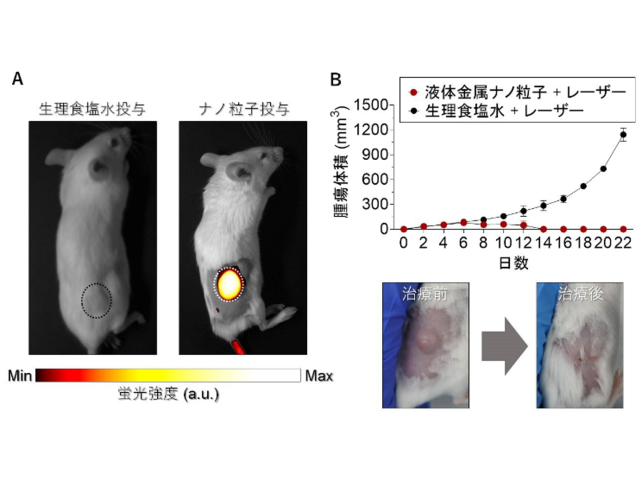
イオン化型白金錯体はヒト臍帯静脈内皮細胞に対して高い光細胞毒性を示す一方,ヒト乳腺上皮細胞株(MCF10A),ヒト乳癌細胞株(MDA-MB-231)に対しては光細胞毒性を示さないことが明らかとなった。腫瘍形成や転移に重要である血管内皮細胞に対するイオン化型白金錯体の選択的光細胞毒性は,正常組織を損傷することなく,腫瘍血管を正常血管にする可能性,すなわち,腫瘍血管の正常化に有用だという。
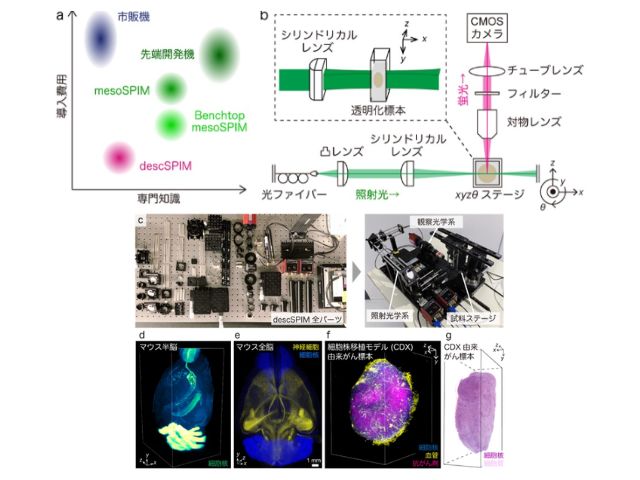
タンパク質内包型白金錯体については,ヒト細胞に対する優れた送達能力が明らかとなったため,研究グループは,生体に対する次世代バイオイメージング材料としての応用が期待できるとしている。