 東京工業大学の研究グループは,細胞内タンパク質結晶化反応を用いて,CO2還元活性を有するギ酸脱水素酵素(FDH)と光増感剤であるエオシンY(EY)の両方を組み込んだハイブリッド固体触媒の合成に成功した(ニュースリリース)。
東京工業大学の研究グループは,細胞内タンパク質結晶化反応を用いて,CO2還元活性を有するギ酸脱水素酵素(FDH)と光増感剤であるエオシンY(EY)の両方を組み込んだハイブリッド固体触媒の合成に成功した(ニュースリリース)。
タンパク質結晶は多孔質構造を形成するため,ゲスト分子を内部に固定化することができる。これまでに,金属クラスター,金属錯体触媒,天然酵素などがタンパク質結晶に固定化されてきた。このタンパク質結晶に複数の機能性分子をカプセル化したハイブリッド材料が実現できれば,多くの応用が期待できる。
しかし,現在のタンパク質結晶のカプセル化システムで扱えるのは,低分子か,単純な触媒反応を行なう酵素に限られており,ハイブリッド材料としての可能性は十分に検討されてこなかった。
研究グループは,多角体の細胞内タンパク質結晶化反応と遺伝子工学的手法を組み合わせることにより,複数の機能性分子を内包したハイブリッドタンパク質結晶材料を合成した。
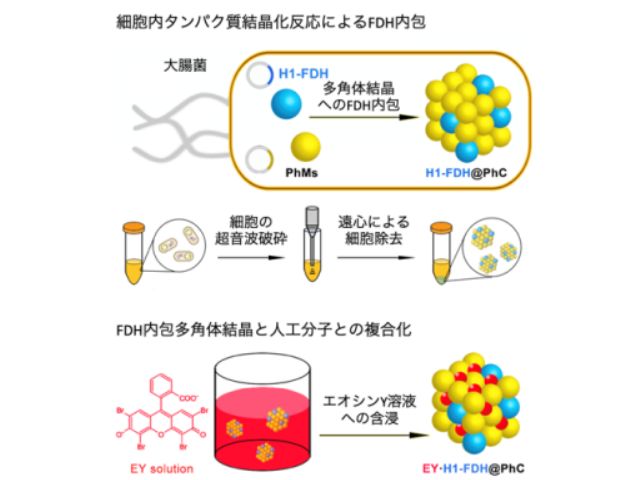
はじめに1つの大腸菌細胞内で,多角体タンパク質と生体分子であるH1-FDHを同時に産生させることによって,自発的にH1-FDHを内包した多角体複合結晶(H1-FDH@PhC)を得ることに成功した。
次に,その複合結晶を光増感剤である人工分子のエオシンY(EY)の溶液に含浸させることによって,H1-FDHとEYの両方をカプセル化した,人工光合成を実現するハイブリッド固体触媒(EY・H1-FDH@PhC)の調製に成功した。
このEY・H1-FDH@PhCハイブリッド固体触媒を用いて,NADH存在下でのカスケード人工光合成反応を行なったところ,光存在下でCO2固定化を達成できることが分かった。
特に,FDHの集積に有利な大きな細孔を形成し,負電荷を有するEYの結合を安定化させる正電荷アミノ酸の変異を導入したPhCd38-K58G/G60K/E63K変異体では,触媒活性の向上が確認された。触媒機能については,PhCに固定化されたFDHは,溶液中のFDHと比較して,ギ酸の酸化反応では94%の触媒活性を示すことが分かった。さらに,タンパク質結晶が内包FDHの再利用性を著しく向上させることも示された。
今回,人工光合成を促進するハイブリッド固体触媒を開発することに成功した。こうしたハイブリッド材料の構築は,ナノ材料や人工光合成の分野において,環境低負荷で高効率な合成戦略が可能となる。
タンパク質精製や材料への固定化といった煩雑な操作が不要であり,研究グループは,新たな固体触媒材料への展開が期待されるとしている。