 理化学研究所(理研)の研究グループは,クライオ電子顕微鏡および大型放射光施設「SPring-8」などの放射光を用いて,タンパク質やその複合体などの生体分子を構成する原子のイオンの「散乱因子」を決定した(ニュースリリース)。
理化学研究所(理研)の研究グループは,クライオ電子顕微鏡および大型放射光施設「SPring-8」などの放射光を用いて,タンパク質やその複合体などの生体分子を構成する原子のイオンの「散乱因子」を決定した(ニュースリリース)。
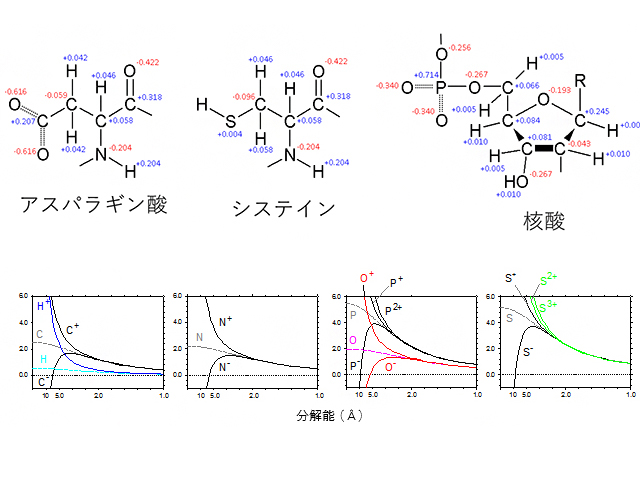
生体分子の構造は,X線や電子線を試料に照射し,その散乱から得られる回折パターンや分子像から調べることができる。X線や電子線の散乱のされ方を散乱因子といい,元素によって決まっている。タンパク質を構成するアミノ酸やDNA,RNAなどの核酸は,水素,炭素,窒素,酸素,リン,硫黄の原子から構成されるが,このうち酸素を除いて,イオンの散乱因子は求められていなかった。
これらのイオンは自然界で安定に存在できないが,分子中では複数の原子にわたり電荷が分布するため,部分電荷を持つ原子の散乱因子をイオンと中性の原子の散乱因子から見積もることが必要になる。さらに,イオンと中性の原子の間で電子線に対する散乱因子に大きな違いがあり,この特徴を利用して電荷の可視化に利用できるなど有用性は高いと考えられるとしている。
今回,研究グループは,生体分子を構成する原子のイオンの散乱因子を「相対論的量子化学計算」から決定した。最近のクライオ電子顕微鏡の発展に伴い,原子のイオンの散乱因子の重要性は増していくという。
今後,イオンの散乱因子を用いて,タンパク質などの生体分子の立体構造,電荷分布の精密解析ができるようになれば,生体分子の作動メカニズムをより深く解明することにつながり,生命科学の発展,新たな治療法や薬の開発,工学などへの応用が期待されるとしている。