 大阪大学の研究グループは,組織深部の観察が可能な2光子励起顕微鏡を用いて,生きたままの骨の内部を観察し,新しい骨を造る“骨芽細胞”と古い骨を溶かす“破骨細胞”を同時に可視化する技術を開発した(ニュースリリース)。その結果,生体骨組織内において,骨芽細胞と破骨細胞が直接接触しコミュニケーションをとる瞬間を捉えることに世界で初めて成功した。
大阪大学の研究グループは,組織深部の観察が可能な2光子励起顕微鏡を用いて,生きたままの骨の内部を観察し,新しい骨を造る“骨芽細胞”と古い骨を溶かす“破骨細胞”を同時に可視化する技術を開発した(ニュースリリース)。その結果,生体骨組織内において,骨芽細胞と破骨細胞が直接接触しコミュニケーションをとる瞬間を捉えることに世界で初めて成功した。
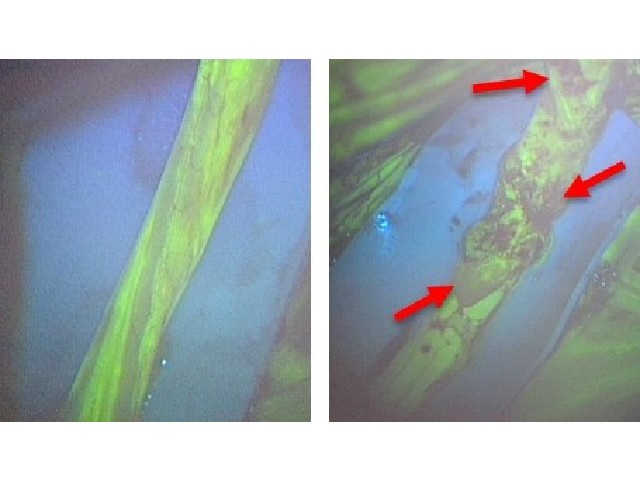
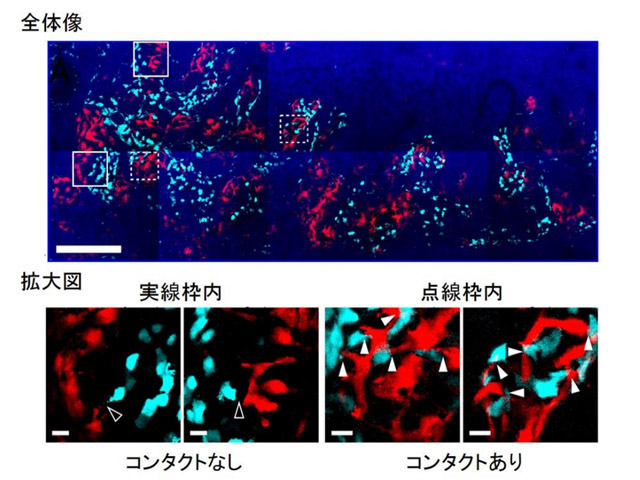
研究グループは,独自に立ち上げてきた骨組織のライブイメージング系を活用して,生きたまま骨の内部の骨芽細胞と破骨細胞を同時に可視化することに成功した。その結果,骨芽細胞と破骨細胞はそれぞれ数十細胞単位で小集団を形成しており,両者の境界部分のほとんどは細胞同士の接触が観察されなかったが,一部の領域において骨芽細胞と破骨細胞が直接接触しコミュニケーションをとることが明らかとなった。
この細胞間コミュニケーションの多くは,破骨細胞の突起が神経シナプス様に骨芽細胞に伸びた構造を呈しており,時間の経過とともに細胞の形態が変化していく様子が観察された。
さらに,骨芽細胞と破骨細胞の細胞間コミュニケーションの生物学的意義を明らかにするために,破骨細胞が出す酸を感知し蛍光がOnとなるpH応答性蛍光プローブを活用してライブイメージングを行なった。その結果,骨芽細胞と接触している破骨細胞では,骨を溶かす機能が低下していることが分かった。これにより,骨芽細胞と破骨細胞の物理的な接触が骨リモデリングの調節に重要な役割を担っていることが明らかとなった。
最後に,研究のライブイメージング技術を薬効評価系として応用し,検討を行なった。骨粗鬆症薬として臨床応用されているものの,その作用機序がよく分かっていない副甲状腺ホルモン(PTH)製剤に注目し,生体骨組織内においてPTH製剤が骨芽細胞および破骨細胞に与える影響を解析した。その結果,PTH製剤を連日投与した群では,薬剤を投与してない群と比較して,骨芽細胞と破骨細胞の細胞間相互作用が有意に増加し破骨細胞の骨を溶かす機能が抑制されていることが明らかとなった。これにより,PTH製剤が生体内で骨量を増加させる仕組みが細胞レベルで明らかとなった。
これらの成果により,骨粗鬆症やがんの骨転移など骨の構造が破綻する病気に対して,骨芽細胞と破骨細胞のバランスを調節するという新たな治療法開発が期待されれるとしている。