 京都大学と東ソーは,芳香族ニトロ化合物と有機ホウ素化合物をカップリングさせる画期的な新反応の開発に成功した(ニュースリリース)。
京都大学と東ソーは,芳香族ニトロ化合物と有機ホウ素化合物をカップリングさせる画期的な新反応の開発に成功した(ニュースリリース)。
鈴木ー宮浦カップリング反応は,有機ホウ素化合物と有機ハロゲン化物を連結させて,新しい炭素ー炭素結合を構築するための反応。特に,ベンゼン環同士を連結させてビアリール化合物を合成する方法として極めて有用で,医薬,農薬,液晶,有機EL材料の工業的生産に用いられている。
この鈴木ー宮浦クロスカップリングの改良が世界中で研究されており,カップリング剤として用いる芳香族ハロゲン化物から腐食性や毒性を持つ廃棄物を生じることがあるため,その代替カップリング剤の開発が特に注目されている。
さまざまな代替候補のなかでも芳香族ニトロ化合物は,芳香族ハロゲン化物を含むさまざまな芳香族化合物の工業的製造プロセスにおける川上原料であるため,これを直接鈴木ー宮浦クロスカップリングさせることができれば,従来の化学プロセスを格段に短工程化できるものと期待されているが,これまで実現できなかった。
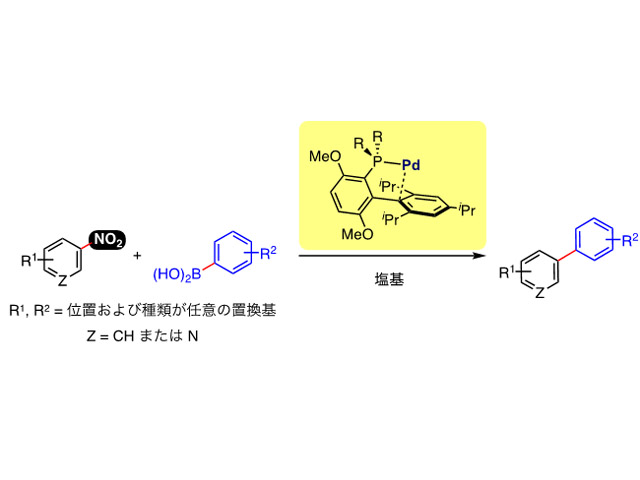
芳香族ニトロ化合物を鈴木ー宮浦カップリングさせるうえでの鍵は,芳香族炭素ーニトロ基結合をいかに切断するかという点。しかし,ニトロ基は,クロスカップリング反応に用いられるような金属触媒を酸化して失活させてしまう性質もあるため,この切断反応に適切な触媒を見つけることは極めて困難だった。
研究グループは,この切断反応の逆反応,すなわち芳香族炭素ーニトロ基結合の形成に有効であると以前に報告されたパラジウム触媒に注目し,この触媒のリン原子上の置換基を改変することによって芳香族ーニトロ基結合の切断を達成し,芳香族ニトロ化合物の鈴木ー宮浦カップリングの開発に成功した。
先述のように芳香族ニトロ化合物は,さまざまな芳香族化合物の出発原料であるため,極めて豊富なバリエーションが市販品として入手できる。また,芳香族ニトロ化合物は,ニトロ基を保持したまま,芳香環上に置換基を導入する反応が行なえるため,そのような反応と今回開発した反応を連続して行ない,多置換芳香環を極めて効率よく合成するような有機合成プロセスの構築が可能になる。
今回開発した芳香族ニトロ化合物の鈴木ー宮浦クロスカップリング反応は,従来有機ハロゲン化物を用いて行なわれている化学プロセスに取って代わって,さまざまな医薬,農薬,液晶,有機EL材料の工業的製造プロセスに応用できる可能性があるという。
また,今回開発した炭素ー炭素結合形成だけでなく,鍵となる芳香族炭素ーニトロ基結合の切断反応を利用して,炭素ー窒素,炭素ー水素,炭素ーフッ素結合形成などの新反応への展開も期待できるため,多置換芳香族化合物の合成プロセスを刷新できる可能性も秘めている。