東京工業大学と九州大学は,高光安定性かつ低毒性のソルバトクロミック蛍光色素を開発し,約1時間の細胞分裂において,細胞膜中の脂質の組成や流動性を連続撮影することに成功した(ニュースリリース)。
生きた細胞の生体膜中の脂質層の組成や秩序とその時間変化の解析は,細胞接着やシグナル伝達などの生命現象や,がんなどの病態形成の解明の鍵を握っている。しかし,従来用いられてきた蛍光色素には高い毒性や低い光安定性といった問題があり,生きた細胞膜の脂質組成などの長時間観察はこれまで実現されていなかった。
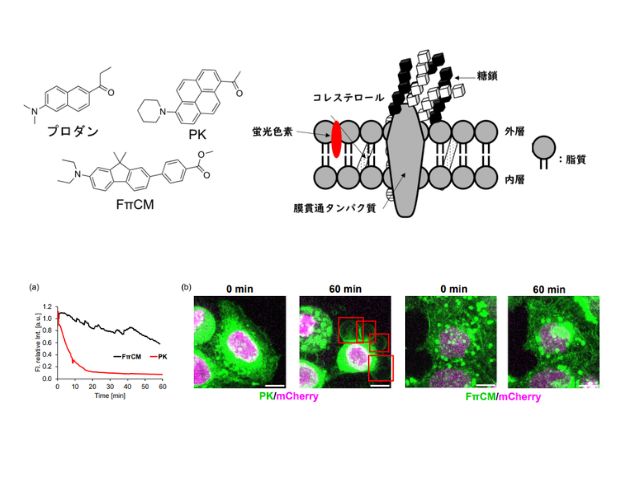
研究グループは,発光特性,光安定性,低毒性のすべての性質を最適化した実用的なソルバトクロミック膜プローブを開発するために,ソルバトクロミック色素の電子受容基として,生体適合性が高いと予想されるカルボン酸エステルを採用し,様々なπ電子系骨格との組み合わせを検討した。
系統的な色素の合成と細胞の染色実験による探索の結果,π共役拡張フルオレン色素FπCMが発光特性,光安定性,低毒性においてバランスの取れた分子設計であることが分かった。
FπCMの蛍光輝度は,標準色素であるプロダンの370の約100倍であり,顕微鏡観察に理想的な色素である。また,蛍光強度の経時変化を調べたところ,光安定性と生体への適合性が高いことが確認できた。
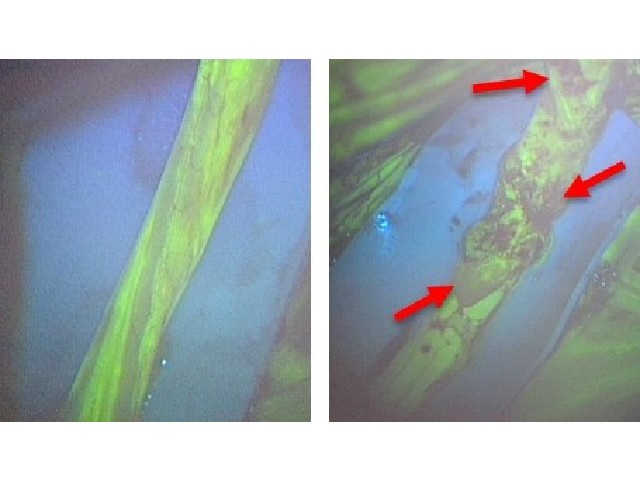
このFπCMを用いて,生命現象の一つである細胞分裂を観察したところ,従来色素のPKでは見られなかった細胞分裂の一部始終の観察に成功した。またFπCMとPKを用いて細胞膜の形態変化を観察したところ,PK観察時には細胞死(アポトーシス)の進行に伴う変化が観察されたが,FπCMではそうした変化は見られず,明らかに細胞毒性が低いことが分かった。
さらにFπCMは,比較的強力なレーザー光を用いても壊れないため,強いレーザー光が必要な超解像顕微鏡での観察も可能であることが確認できた。
研究グループは,この色素は一般的な蛍光顕微鏡だけでなく,数ナノのサイズを判別する超解像顕微鏡にも用いることができ,多様な膜機能の解明,細胞外/細胞内刺激に応答した膜タンパク質の活性化などのメカニズム解明につながるとしている。