九州大学,北里大学,理化学研究所(理研)は,医療応用に向けて最も重要なMRI癌プローブであるピルビン酸の13C核スピンをtriplet-DNPによって高偏極化することに初めて成功した(ニュースリリース)。
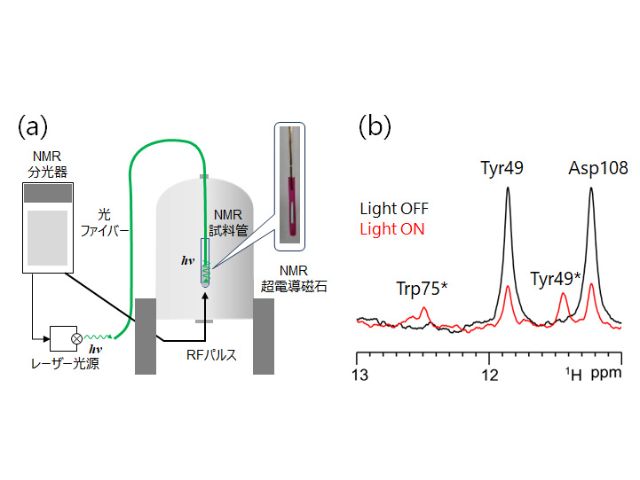
核磁気共鳴分光法(NMR)は非破壊・非侵襲な分析手法だが,その感度は非常に低いため,磁気共鳴イメージング(MRI)では生体内に多量に存在する水分子しか観測できない。
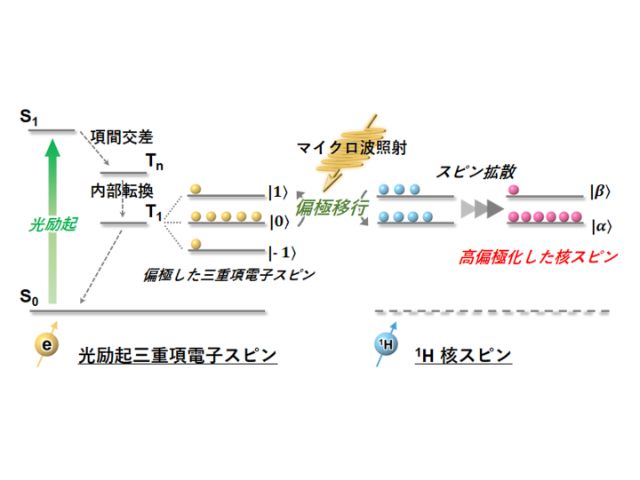
NMRやMRIの感度を向上させる手法の一つとして動的核偏極(DNP)がある。DNPは電子スピンの高い偏極率を核スピンへ移行することで高感度NMR/MRIを実現するが,高磁場・極低温を必要とする。
⼀⽅,電⼦スピンとして特に光励起三重項電⼦スピンを利⽤したtriplet-DNPは穏和な条件下でDNPを実⾏できるが,これまでのtriplet-DNPにおける偏極源分子は主に疎水的なペンタセンが用いられ,偏極移行可能なターゲット分子はペンタセンを分散することができる疎水性分子に限られていた。
高感度MRIへの応用に向けて重要なピルビン酸といった親水性の生体分子プローブとペンタセンは相溶性が悪く,生体分子プローブの核スピンを高偏極化することは困難だった。
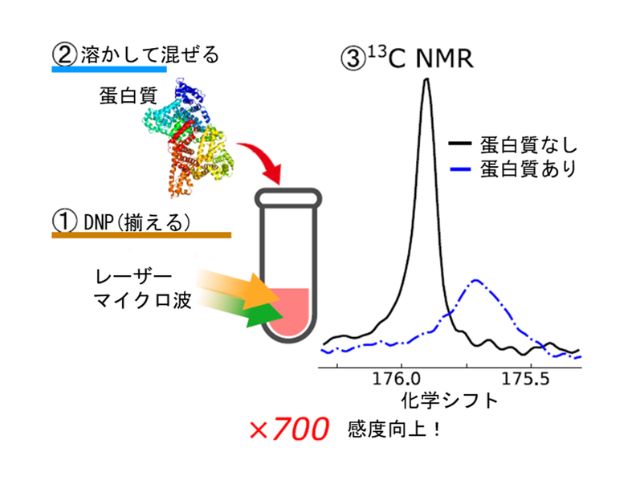
研究グループは,水溶性ペンタセン誘導体(NaPDBA)とβ-シクロデキストリン(βCD)の超分子形成を利用することで,高濃度の[1-13C,d3] ピルビン酸ナトリウム ([1-13C,d3]NaPyr) が溶解した水系ガラスマトリックス(DNP juice)中でも偏極源を分散させることに成功し,triplet-DNPによる[1-13C,d3]NaPyr の13C核スピンを高偏極化することに成功した。
Triplet-DNPによって核スピンを偏極するためには,光励起三重項電子スピンの偏極寿命が十分に長いことが必要。そのため,DNP juice中で極性の高いNaPyrが高濃度に存在する場合,NaPDBAは凝集し,三重項電子スピンの偏極を使うことができない。
そこで,研究グループはNaPDBAとβCDの超分子形成を利用することで,高濃度にNaPyrが溶解したDNP juice中で偏極源NaPDBAを分散させることに成功した。その結果,NaPDBAは十分に長い寿命を有する三重項電子スピンの偏極を生成し,triplet-DNPと交差分極によって[1-13C,d3]NaPyrの13C-NMRを高感度化することに成功した。
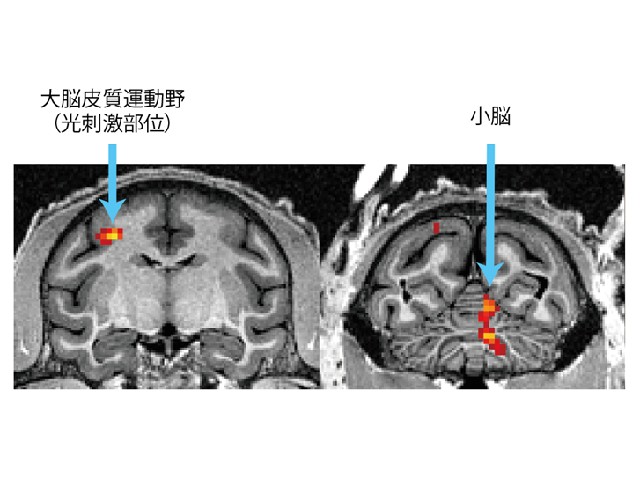
研究グループは,生体分子プローブであるピルビン酸を高偏極化することが可能になり,高感度MRI癌診断を低コストで医療機関へと提供することに繋がるとしている。