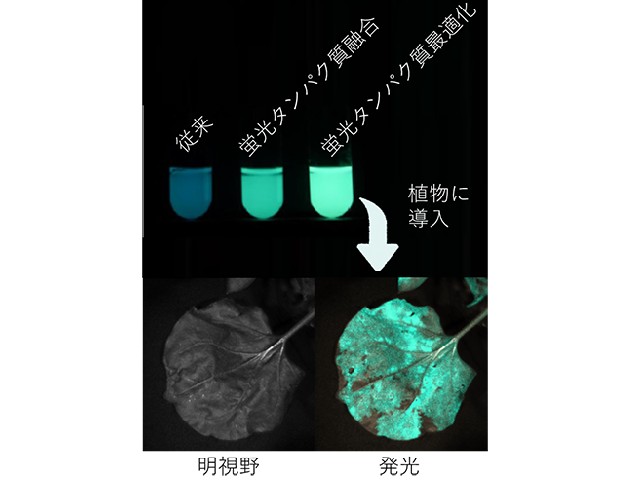
 大阪大学の研究グループは,バクテリア由来の発光タンパク質(Lux)を蛍光タンパク質と融合することで,従来のLuxよりも10倍明るくすることに成功した(ニュースリリース)。
大阪大学の研究グループは,バクテリア由来の発光タンパク質(Lux)を蛍光タンパク質と融合することで,従来のLuxよりも10倍明るくすることに成功した(ニュースリリース)。
蛍などで知られる生物発光は,細胞内の発光タンパク質(ルシフェラーゼ)が基質(ルシフェリン)を酸化する化学反応のエネルギーを利用して光を放出する。
従って,発光タンパク質と基質を細胞内で作ることにより,自ら光ることが可能となる。この様な発光タンパク質を応用することで特定の生命現象を可視化する指示薬(例えばカルシウムセンサ)などを開発し,多くの生物学的知見を得ることに成功している。
これまでに様々な生物種から発光タンパク質が単離されてきたが,発光タンパク質と基質を生合成するための遺伝子がわかっているのは発光バクテリアとヤコウタケのみだという。ヤコウタケの発光タンパク質は比較的明るいものの,30℃を超えると失活し,ヒト細胞(37℃)や30℃以上の環境を要する研究には適さない。
一方,バクテリア由来の発光タンパク質であるLuxは37℃でも失活はしないが,発光強度が低く発光を捉えるために分オーダーの長い露光時間を要するため,分間隔以下で起こる生命現象の変化を捉えることができなかった。明るくなれば,発光を捉えるために要する露光時間が短くなり,速い変化を捉えられることから,発光光度の増強が課題だった。
研究グループでは,黄色蛍光タンパク質VenusをLuxと融合する方法により,高光度化を実現した。これは,発光タンパク質から蛍光タンパク質に発光反応の励起エネルギーを高効率で移動させることにより熱に変換されるエネルギーも光に変換させる原理を利用しだものだという。
さらに,黄色蛍光タンパク質の円順列変異体を利用することにより,このエネルギー移動の効率を最適化し,バクテリアでは10倍,植物では7倍,ヒト細胞では3.5培の高光度化に成功した。
この成果により,発光タンパク質を応用した動物細胞等の高温度域(30℃以上)の自発光を利用したバイオイメージングが広がることが期待される。研究グループは,今回の成果をさらに発展させ,発光色を変える改変などもできれば,生体の深部イメージングなどにも応用できるとしている。