 名古屋大学と京都大学は,記憶や学習に必須でありながら,その異常は脳卒中などの疾患の原因ともなってしまう,脳内たんぱく質のグルタミン酸受容体に対して,蛍光色素などの目印を迅速に付ける(蛍光標識する)手法を開発した(ニュースリリース)。
名古屋大学と京都大学は,記憶や学習に必須でありながら,その異常は脳卒中などの疾患の原因ともなってしまう,脳内たんぱく質のグルタミン酸受容体に対して,蛍光色素などの目印を迅速に付ける(蛍光標識する)手法を開発した(ニュースリリース)。
脳内において,グルタミン酸受容体は記憶や学習に関わる重要なたんぱく質で,その代表例として,AMPA受容体やNMDA受容体が知られている。
グルタミン酸受容体の神経細胞内での動きを知ることは,記憶のメカニズム解明だけでなく,神経疾患の診断方法などにもつながる。そのためには,神経細胞の受容体に蛍光の標識を付けて,記憶の強化や減弱に伴う受容体の発現量の変化を解析できる技術の開発が求められる。
これまでに,蛍光たんぱく質(2008年下村脩氏らのノーベル化学賞)を使ってAMPA受容体やNMDA受容体を蛍光標識する技術が開発されている。しかし,蛍光たんぱく質を用いた方法では,多くの場合において新たに蛍光たんぱく質を標識した受容体を遺伝子工学的に神経細胞内に強制発現させる必要があるだけでなく,蛍光たんぱく質のサイズが大きいために受容体の本来の機能を阻害することも問題となっていた。
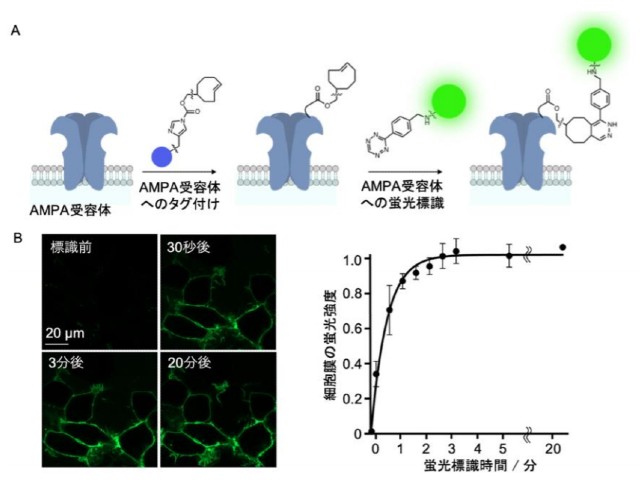
そのような背景のもと,研究グループは,2017年にAMPA受容体に対して蛍光の標識を付けることができる小分子化合物を見いだした。しかし,蛍光標識には2~4時間の時間を必要としたため,受容体の動きの定量的な観察には問題を抱えていた。もし,迅速に蛍光標識することができれば,任意のタイミングで定量的に観察することが可能となる。
今回,AMPA受容体およびNMDA受容体に対して選択的に目印を付けられる新たな有機小分子化合物を開発し,2~3分と従来法に比べて60分の1以下の時間で蛍光標識を実現した。この手法を用いることで,神経細胞でのAMPA受容体およびNMDA受容体の動きの定量解析に成功し,モデル動物細胞に発現させた場合に比べて,受容体たんぱく質の寿命が約6倍と大幅に長くなることを見いだした。
また,この迅速な蛍光標識技術により,神経細胞内ではAMPA受容体が効率的に細胞膜と細胞内を行き来(リサイクリング)することも明らかにした。今後,この蛍光標識技術を用いて受容体の動きを詳細に可視化することで,記憶や学習の脳高次機能の解明だけでなく,神経疾患や精神疾患の原因解明や新たな診断方法の開発につながることが期待されるとしている。