 京都大学と東海大学らの研究グループは,高強度のテラヘルツ光パルスをヒトiPSに照射すると,細胞の中で発現量が変化する遺伝子ネットワークが存在することを発見した(ニュースリリース)。
京都大学と東海大学らの研究グループは,高強度のテラヘルツ光パルスをヒトiPSに照射すると,細胞の中で発現量が変化する遺伝子ネットワークが存在することを発見した(ニュースリリース)。
多能性幹細胞であるiPS細胞は再生医療や創薬技術の開発に期待されている。多能性幹細胞は私たちの体を構成する様々な機能を持つ細胞に分化する可能性を持っていることから,iPS細胞から分化誘導した神経細胞や肝臓などを移植する細胞移植治療への応用が研究されており,近年,iPS細胞を望みの機能を持った細胞に自在に分化させる制御技術の研究が精力的に行なわれている。
一方,電場が生体応答を制御することは古くから知られており,これまで電極を細胞に直接接触させて細胞の応答の変化を調べるという研究が行なわれてきた。今回,このような電極を用いずに高強度テラヘルツ光パルスの発生技術を活用し,非接触で瞬間的に非常に強いテラヘルツ光の持つ電場をiPS細胞内部に印加し,このときに遺伝子ネットワークに及ぼす影響について研究を行なった。
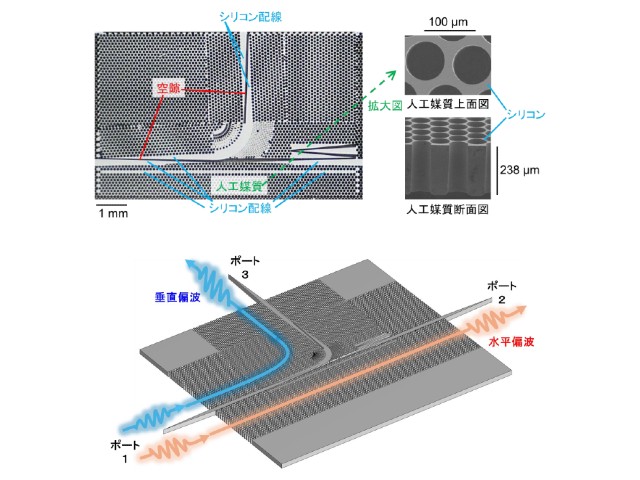
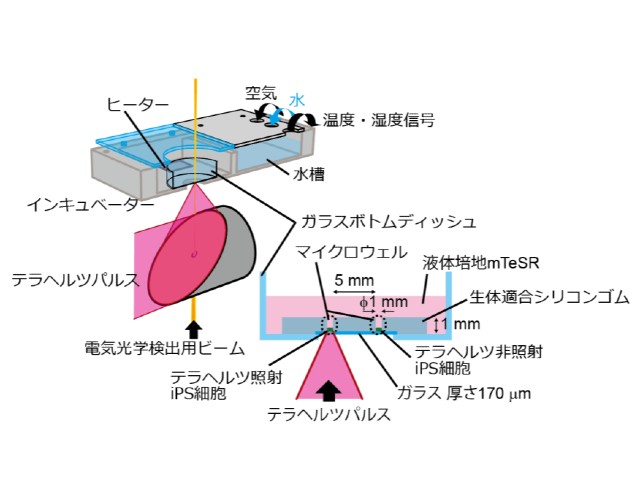
研究では,世界最高レベルのテラヘルツ光パルスを照射することが可能で,またiPS細胞をpHや温度などの最適条件で長時間培養することができる設備を組み合わせた装置を新たに開発した。
この装置を使って,未分化の状態を保ったiPS細胞を培養しながらテラヘルツ光パルスを照射した。この細胞の中から全 RNAを回収し,細胞内に存在するメッセンジャーRNAを網羅的に解析するRNA-seqを使って,テラヘルツパルスの照射の有無による遺伝子発現量を比較した。
その結果,テラヘルツパルス(0.5MV/cm,1kHz)を1時間照射することによって,細胞内で92種の遺伝子発現が上昇,116種の遺伝子の発現が減少し,それらから構成される遺伝子ネットワークが複数存在することを発見した。
さらに,これらの遺伝子ネットワークを構成する各遺伝子の上流には,亜鉛イオンによって活性化するジンクフィンガーと呼ばれる転写因子が多数存在することを見出した。これは,テラヘルツ光パルスの電場が,細胞内における金属イオンの分布を変化させることによって,遺伝子発現を変化させている可能性を示唆すという。
この研究は,iPS細胞の遺伝子発現ネットワークを,テラヘルツ光パルスの照射によって非接触・非侵襲的に変化させることができることを示した世界初の研究成果だとしている。