名古屋大学は,これまで提唱はされてきたものの確認されてこなかった反応中間体「芳香族ラジカルカチオン」の単離と反応機構の解明に初めて成功した(ニュースリリース)。
塩化鉄(III)を用いた酸化的炭素—炭素結合形成反応は,ナノ炭素材料の構築に広く応用される鍵反応の一つ。例えば,有機半導体,太陽電池などの機能が期待されるヘキサベンゾコロネンやナノグラフェンなどの合成最終段階で現在でも使用されている。しかし,100年以上の歴史を持つ信頼性の高い反応にもかかわらず,反応機構は未解明のままだった。
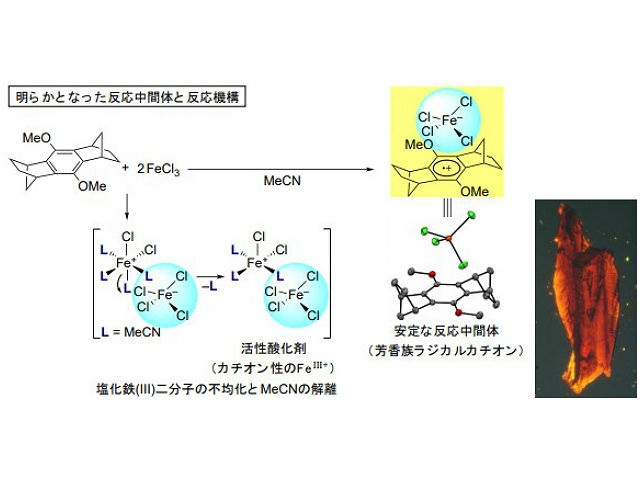
今回,研究グループは,立体的に混み合った芳香族化合物を用いることで,短寿命とされる芳香族ラジカルカチオンを安定化し,X線構造解析や紫外可視分光法(UV-vis)等を用いて構造を決定した。さらに反応速度論解析により,芳香族ラジカルカチオンの生成メカニズムも明らかにした。明らかにした反応機構では,提唱されている一分子のIIIによる酸化反応ではなく,「III二分子の不均化」と「MeCNの解離」により生成したカチオン性のFeIII+であることを解明した。
さらに,得られた知見を基に,芳香族ラジカルカチオンを鍵中間体とする[4+2]環化反応と[2+2]環化反応の2つの反応開発への応用に成功した。医農薬に多く見られるシクロヘキセン環およびシクロブタン環を構築できる有用な反応だが,酸触媒や熱によって反応が進行しない基質(出発原料)があり,大きな課題となっていた。
今回,IIIから生成できる芳香族ラジカルカチオンを鍵中間体とすることにより,この課題を克服した。触媒量のIIIを開始剤とするMeCN溶媒中での2つの環化反応では,既存の開発例と比べて幅広い基質適用範囲を示した。さらに,三角フラスコを用いた常温,常圧,空気存在下,100グラムスケールでの大量合成にも適用できることを確認した。
多くの有機合成反応で必要とされる不活性雰囲気を必要としないことに加えて大スケールでも問題なく反応が進行することから,実用性の高さと工業的生産の可能性を示している。とりわけ合成できた[4+2]環化反応の生成物は,さまざまな医薬品に含まれるシクロヘキセン骨格を構築できることからその有用性が期待できるという。
研究グループは,今回解明した反応機構を基に,鉄(III)塩の最適化や助触媒の添加などの検討をすることで,ナノ炭素材料の収率向上と合成の効率化,さらには既存の方法では合成の難しかった新規ナノ炭素材料の開発にも繋がるとしている。