 大阪市立大学の研究グループは,動物の非視覚機能に関する光受容タンパク質の一つである「ペロプシン」が,一般的な光受容タンパク質と真逆の特性を有することを明らかにした(ニュースリリース)。
大阪市立大学の研究グループは,動物の非視覚機能に関する光受容タンパク質の一つである「ペロプシン」が,一般的な光受容タンパク質と真逆の特性を有することを明らかにした(ニュースリリース)。
動物は視覚に関するものと,そうでないのもの,さまざまな光受容タンパク質を持つ。たとえば,ヒトは9つの光受容タンパク質の遺伝子を持っている。そのなかで,4つは視覚の機能に,残りの5つは非視覚の機能に関わると考えられているが,具体的な機能は完全には明らかになっていない。
今回,これら5つの非視覚の光受容タンパク質の一つで,無脊椎動物にも存在している「ペロプシン」と名付けられた光受容タンパク質が,これまでに知られていない特徴を持つことを明らかにした。
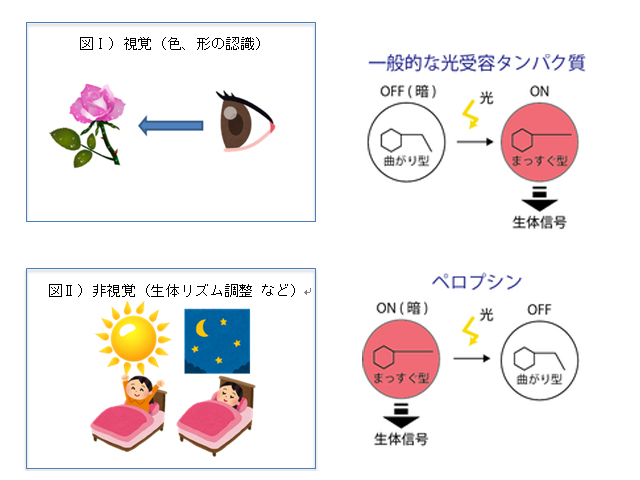
光受容タンパク質は,光をキャッチするためにビタミンAの仲間(レチナール)を補助的な分子として結合している。視覚の光受容タンパク質は「曲がり型」の補助分子を結合していて,光をキャッチするとこれが「まっすぐ型」に変化し,光受容タンパク質がON型となり,それが引き金となり生体信号が生じる。
一方,ペロプシンは視覚の光受容タンパク質とは全く逆の振る舞いをすることを見出した。実験の結果,ペロプシンは,暗中では「まっすぐ型」の補助分子を結合しON型であり,生体信号を生じさせているが,光をキャッチすると発色団が「曲がり型」に変化してOFF型になることが示唆された。
すなわち,一般的な光受容タンパク質は「暗で不活性,光で活性化」であるのに対して,ペロプシンは「暗で活性,光で不活性化」というユニークな光受容タンパク質である可能性を見出した。ペロプシンは,一般的には目に存在するが,具体的にどのような機能に関わっているのかは,ほとんど明らかになっていない。今後,研究により発見された「真逆の分子特性」を入り口として,機能解明が進むと期待される。
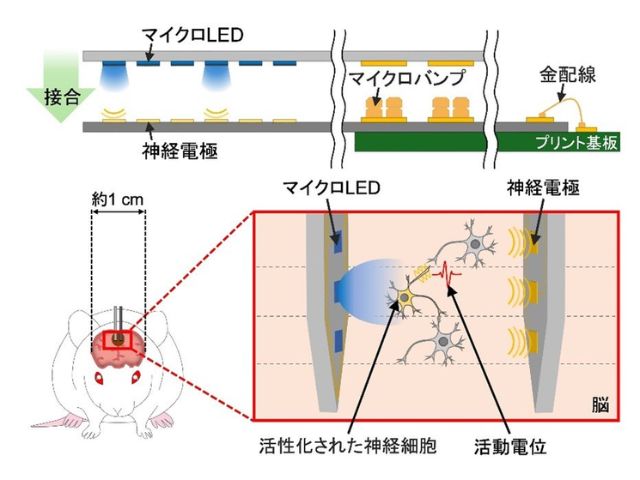
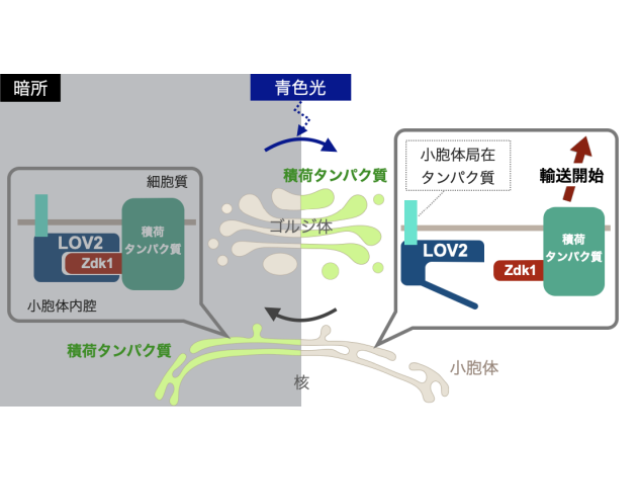
また,近年,遺伝子組み換え技術と光受容タンパク質を利用した新しい技術である光遺伝学が注目されている。光遺伝学では,実験動物の狙った細胞に光受容タンパク質を持たせておき,光を当てることで,生きた動物の中で狙った細胞の活動を制御できる。これにより,特定の神経細胞などの機能を動物の行動と結びつけて明らかにすることが可能となる。
生体内の細胞はさまざまな生体信号により多様な活動パターンを示すことから,細胞の活動を意図的に制御するためにはさまざまな性質を持つ光遺伝学ツールが必要となる。今回発見されたペロプシンの光でオフになる性質を利用すれば,「神経細胞を刺激なしに興奮状態に保ち,光により不活性化する」ことが可能となるので,新たな光遺伝学ツールとして注目されるとしている。