 国立医薬品食品衛生研究所は,日本医療研究開発機構(AMED)および先端医療振興財団との共同研究により,再生医療用の移植細胞の製造中に混入または発生するがん化のリスクを持つ悪性形質転換細胞(がん細胞)を超高感度に検出する方法「デジタル軟寒天コロニー形成試験法」を開発した(ニュースリリース)。
国立医薬品食品衛生研究所は,日本医療研究開発機構(AMED)および先端医療振興財団との共同研究により,再生医療用の移植細胞の製造中に混入または発生するがん化のリスクを持つ悪性形質転換細胞(がん細胞)を超高感度に検出する方法「デジタル軟寒天コロニー形成試験法」を開発した(ニュースリリース)。
再生医療に用いられる移植細胞の製造における大きな懸念の一つに,細胞サンプルが誤って混ざってしまうリスク(クロス・コンタミネーションのリスク)がある。中でもがん細胞が混ざってしまうことは重要な問題となる。このような問題に対処するため,移植細胞の製造工程管理においてがん細胞の存在を否定しする方策が求められる。
がん細胞の特性の一つである足場非依存性増殖を利用する軟寒天コロニー形成試験は,正常細胞中に混入する悪性形質転換細胞の存在を比較的短期間かつ簡便に評価することが可能な試験だが,従来法は検出感度が低いという問題があった。
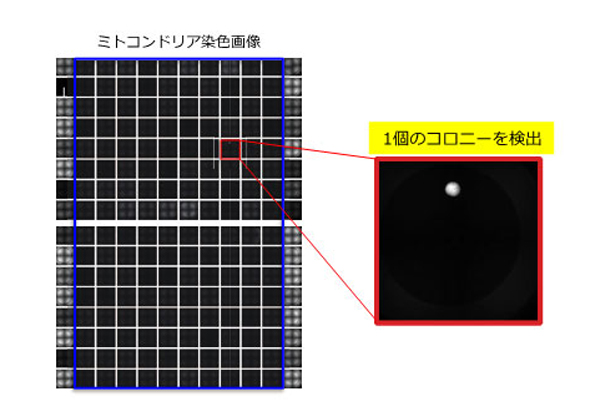
そこで,研究では画像解析によるコロニー検出法の確立を試みた。その結果,細胞の核,ミトコンドリアをそれぞれ青,赤に染める生細胞染色試薬を用いてコロニーを染色し,コロニーの形状,大きさ,蛍光輝度等を指標とすることで,1個のコロニーを高精度に認識することが可能となった。さらに,ハイコンテンツイメージングシステムを利用することで,画像解析のハイスループット化(大量迅速処理)にも成功した。
次に,この技術を応用し,再生医療用の移植細胞中に混在するがん細胞の新たな検出法,デジタル軟寒天コロニー形成試験を考案した。これは,細胞試料をマルチウェルプレートに分割,播種して軟寒天培養を行ない,各ウェル内での細胞コロニー形成を解析し,足場非依存的に増殖するがん細胞の混入を評価する手法。
この試験法により,高シグナル/ノイズ比が確保され,試料中にごく微量に存在するがん細胞を高感度に検出することが可能となる。また,ハイコンテンツイメージングシステムを利用した解析を行なうことで,画像解析のハイスループット化も可能と考えた。
試験の結果,1000万個のヒト間葉系幹細胞中に存在する1個のHeLa細胞由来のコロニーを6回の試行中4回検出することに成功した。この結果は,HeLa細胞相当のがん細胞が混入する細胞試料であれば,0.00001%の感度で検出可能であることを示唆するものであり,従来の手法による検出感度と比較して1万倍の感度向上を実現させた。
また,細胞試料を分画,播種するウェル数及び培養細胞数を調節することで,検出感度を適宜向上させることが可能であることに加え,細胞数にかかわらず,高検出感度を保持するこの試験法の適用が可能であることも考えられるという。
今後は,再生医療用の移植細胞の製造工程における品質評価のための標準的な試験系にすることを目指し,試験系の自動化等もふまえ,試験方法の最適化に向けた研究を進めていくとしている。
関連技術「産総研,腫瘍となるヒトiPS/ES細胞を除く技術を開発」「近大ら,レーザを用いたiPS細胞の品質を維持する装置を開発」「京大など、細胞移植に適した新しいヒトiPS細胞の樹立・維持培養法を確立」






























