 国立循環器病研究センター,高輝度光科学研究センター,大阪大学らの研究グループは動物実験により,心臓に移植されたiPS細胞由来心筋細胞内の収縮タンパク質分子が,宿主心筋と同期して運動することを,最先端の放射光ナノ技術を用いて世界で初めて証明した(ニュースリリース)。
国立循環器病研究センター,高輝度光科学研究センター,大阪大学らの研究グループは動物実験により,心臓に移植されたiPS細胞由来心筋細胞内の収縮タンパク質分子が,宿主心筋と同期して運動することを,最先端の放射光ナノ技術を用いて世界で初めて証明した(ニュースリリース)。
これまで動物実験により,iPS細胞を心筋細胞に分化誘導させた自己拍動するiPS細胞由来心筋細胞の傷害心臓への移植で,心臓機能が改善することが報告されてきた。しかしながら,移植されたiPS細胞由来心筋細胞が収縮弛緩を示し,宿主心臓と電気的に接合し同期運動することにより心臓機能改善に寄与するという,心筋再生における最も重要なメカニズムは証明されていなかった。
研究グループは,ラットの心筋梗塞巣に移植されたiPS細胞由来心筋細胞内の収縮タンパク質分子(アクチン,ミオシン)が,宿主心臓と同期しながら運動を続けていることを,放射光X線回折法のラット拍動心臓への応用により,直接的に映像化することで証明した。
この手法は,心臓収縮の力の源となる心筋の収縮タンパク質分子の運動を,心室の様々な部位においてピンポイントで評価可能とする放射光X線回折法であり,平成25年1月に国立循環器病研究センターと高輝度光科学研究センターが発表したもの。
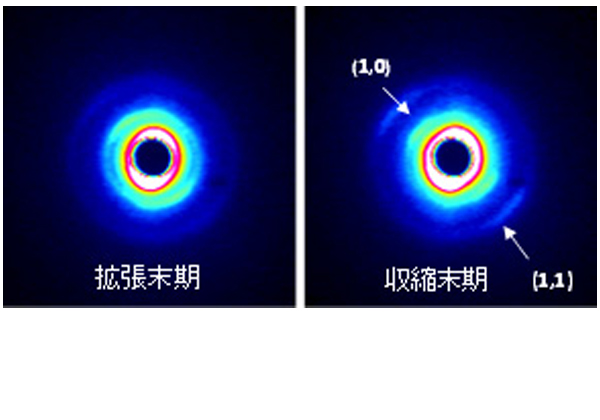
今回の研究では,まずラット心臓の左冠状動脈を結紮することによって心筋梗塞を発生させた。次に,ここへ心筋に分化させたiPS細胞由来心筋細胞培養シートを移植した。その後,iPS細胞由来の心筋細胞が宿主心臓と融合した頃に,大型放射光施設SPring-8の高輝度放射光を用いたX線回折実験により,これら細胞内の収縮タンパク質に由来するX線回折ピークを観察した。
これらの回折ピークの強度は心筋の収縮と同期して変化しており,収縮タンパク質が心臓と同期して働き,張力を発生していることが明らかになった。これは,移植されたiPS細胞由来の心筋細胞が,宿主心臓と電気的に接合して同期運動していることを証明するもの。この実験結果は,iPS細胞由来の心筋細胞が心臓の一部となって働いていることを示しており,心筋再生による心臓機能の改善が見込まれる。
iPS細胞を用いた心筋再生治療を実現化するために,その治療効果のメカニズムを明確にすることは極めて重要となる。この研究では,世界最先端の放射光技術を用いて,心臓に移植されたiPS細胞由来心筋細胞の収縮弛緩を,心臓収縮の力の源となる分子レベルの心筋収縮タンパク質分子の運動で捉えることができた。
今回,iPS細胞をSPring-8で評価するという二分野の本邦発の最先端技術を融合させることで,心臓疾病に対する次世代型治療を開発する上で非常に重要なエビデンスを示した。研究グループは今後,このような異分野間の連携により科学の進歩が加速されるとている。
関連記事「東大ら,タンパク質断片の1分子内部動態を高速X線回折像からリアルタイム動画撮影に成功」「慶大と理研,SACLAのコヒーレントX線回折イメージングデータを高速処理するソフトを開発」






























