放射線医学総合研究所 分子イメージング研究センター 分子神経イメージング研究プログラム 脳分子動態チームチームリーダーの樋口真人氏らは,世界で初めて脳内でのタウ(神経系細胞の骨格を形成する微小管に結合するタンパク質。アルツハイマー病をはじめとするさまざまな精神神経疾患において,異常にリン酸化して細胞内に蓄積することが知られている。)の蓄積をPETにより画像化することに成功。タウの蓄積とアルツハイマー病の重症度の関連性を示唆する成果も得た。
さらに,アルツハイマー病以外の認知症でのタウの画像化においても有効であるとの成果を得ることができ,多様な認知症についての発症メカニズムの解明や,症状からの診断が困難である発症初期の診断,重症度の客観的な診断,認知症治療薬の開発促進が期待される。
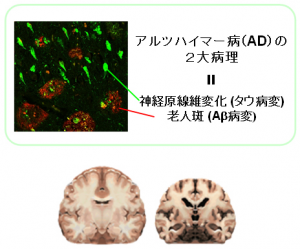
近年,認知症患者の増加が社会問題となっているが,発症原因は不明な点も多く,効果的な治療法は確立されていない。国内の全認知症患者の半数にのぼるとされるアルツハイマー病患者の脳内では,アミロイドベータ(Aβ)(アルツハイマー病やダウン症候群にみられる病理学的変化である老人斑,脳アミロイド血管症(アミロイドアンギオパチー)の主成分の1つ。Aβ自身も神経細胞に毒としての作用を及ぼすことが報告されている。)やタウの蓄積に伴い神経細胞が死ぬことで,物忘れなどの症状が発現していく。
アルツハイマー病の確定診断は脳内において,これら異常タンパク質の蓄積を確認することが必要だが,これまでは患者の死後に脳切片を染色して顕微鏡で見ることで,確認できるものだった。その状況を変えたのがPETによる生体内でのAβの画像化技術だすが,タウの画像化は未開発であった。
今回,放医研は,タウの蓄積を画像化するPET薬剤(PBB3)を開発し,認知症モデルマウスとヒトで脳内タウ病変を明瞭に画像化した。アルツハイマー病患者では,疾患の進行に伴うタウ蓄積部位の拡大が明らかに確認でき,皮質基底核変性症という異なる種類の認知症のタウ病変も画像化できた。
この研究の成果により,発症初期からの認知症の鑑別診断,および疾患の進行度の客観的評価が可能になった。これまでは,神経細胞死に密接に関わるのは神経の外に蓄積するAβであると考えられていたが,最近の研究により,より影響を与えているのは神経の中に蓄積するタウであるという考えが強くなっていることから,PBB3はモデルマウスを活用したタウ蓄積抑制治療薬の評価や,その後のヒトでの新規治療薬の評価など,認知症の根本治療法の開発への貢献も期待される。
詳しくはこちら。