2重膜を形成している動物細胞の細胞膜で、フォスファチジルセリンやフォスファチジルエタノールアミンのリン脂質は膜の内側にのみ存在するが、フォスファチジルコリンは外膜に多く存在する。この膜の非対称性は種々の局面で破綻する。例えば、出血により活性化された血小板はフォスファチジルセリンをその表面に暴露し、このフォスファチジルセリンが血液凝固因子を活性化、血液を凝固させる。
一方、細胞がアポトーシス(細胞死)に陥るとフォスファチジルセリンが暴露され、これをマクロファージが死細胞からの「eat me」シグナルと認識し、死細胞を貪食する。リン脂質の非対称性を崩壊させる分子はスクランブラーゼ(Scramblase)と呼ばれているが、その実体は明らかではなかった。
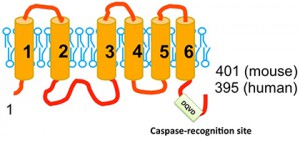
京都大学医学研究科助教の鈴木淳氏、教授の長田重一氏、教務補佐員の今西英一氏らのグループは、アメリカマサチューセッツ工科大学教授のH. Robert Horvitz氏、Daniel P. Denning氏のグループと共同で、このフォスファチジルセリン暴露の過程に関与している膜蛋白質(Xkr8)を同定した。
このXkr8は増殖している細胞中では活性のない前駆体として存在し、アポトーシスがおこるとカスパーゼによって直接、切断活性化される。フォスファチジルセリンは貪食細胞が死細胞を貪食するためのシグナルであり、フォスファチジルセリンが提示されないと、死細胞は貪食されず、細胞膜が破裂、いわゆるネクローシス状態に陥ると考えられる。
研究グループは2種のヒト白血病細胞でXkr8遺伝子のプロモーターがメチル化され、その発現が抑制されていることを見いだした。このようながん細胞はアポトーシスに陥っても貪食されず、ネクローシスに陥った細胞から放出された細胞内分子により、強い炎症反応が惹起される可能性がある。このことががんの進行を引き起こす可能性がないかどうかが今後の課題となる。
詳しくはこちら。