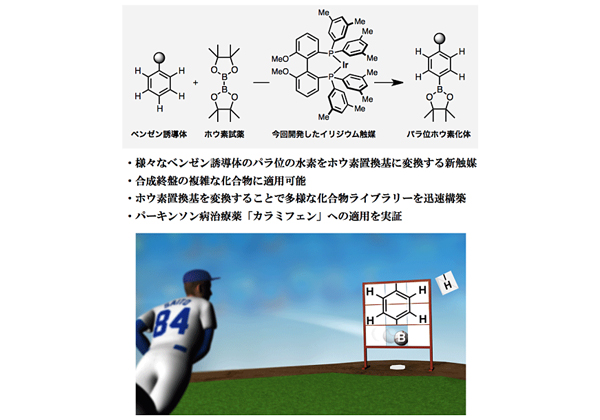
 名古屋大学は,長らく達成できなかったベンゼン環のパラ位の水素をホウ素に変換する新触媒を開発し,合成化学の新しい方法論を樹立することに成功した(ニュースリリース)。
名古屋大学は,長らく達成できなかったベンゼン環のパラ位の水素をホウ素に変換する新触媒を開発し,合成化学の新しい方法論を樹立することに成功した(ニュースリリース)。
ベンゼン環に結合している水素原子を様々な置換基に置き換えることで,ベンゼンに多彩な機能を付与することができる。6つの水素を別の置換基に置き換えていくとき,2つ目の置換基のつき方は3種類あるが,それぞれ性質が異なるため,狙ったところに置換基を導入する方法が求められてきた。特に,1つ目の置換基から最も遠い位置(パラ位)は,化合物全体の形や性質を大きく変えるため最も重要だが,同時に選択的に置換基を導入することが最も難しく,汎用的なパラ位変換反応はこれまで不可能だった。
研究グループは,ベンゼン環のパラ位にホウ素の置換基を選択的に導入する方法を開発した。ホウ素の置換基は,鈴木−宮浦クロスカップリング反応などによって様々な置換基に簡便に変換できるため,パラ位ホウ素化体を起点として多種多様な誘導体へと変換することが可能となる。
イリジウム触媒を用いてベンゼン環上の水素をホウ素化する反応がよく知られているが,ベンゼン環上の置換基が1つの場合は,メタ位とパラ位の両者にランダムに反応してしまうという欠点があった。研究グループは,触媒を適切に設計すれば,パラ位選択的なホウ素化反応が実現できると考えた。特にイリジウムに配位して触媒の性質を制御する「配位子」に着目し,これまで主に用いられていた窒素系配位子の他にリン系配位子も数多く試した。
その結果,かさ高い二座リン配位子を用いた場合に,パラ位のホウ素化が最大91%と高選択的に進行することを発見した。これは,イリジウム周りがかさ高くなったために,置換基と配位子の立体反発によりメタ位の炭素水素結合がイリジウムと反応しにくくなったためと考えられる。実際に,ベンゼン環上の置換基をだんだん小さくしていくとパラ位の選択性が下がっていくことが分かった。
今回開発したパラ位ホウ素化反応の有用性は,パーキンソン病治療薬「カラミフェン」の迅速誘導化へ応用することによって実証された。反応は,カラミフェンのアミノ基やエステルといった極性官能基の存在下でも問題なく進行し,目的とするパラ位ホウ素化体を選択的に得ることに成功した。これに対して既存のホウ素置換基変換反応を適用することで,それぞれわずか2段階で5種類のカラミフェン誘導体を合成することに成功した。
カラミフェンのようにベンゼン環をもつ医薬品化合物や機能性材料化合物は無数に存在する。それら医薬品や機能性材料のベンゼン環のパラ位を変換することで,その性能・機能を大きく変える可能性を秘めていることから,今回開発した方法は非常に画期的であり合成化学の戦略を一変させる可能性があるものだとしている。
関連記事「筑波大、ベンゼン環を開裂させる反応を世界で初めて発見」「名大,置換ベンゼンを意のままにつくる新しい合成法を開発」「理研,ベンゼンの「炭素-炭素結合」を室温で切断することに成功」





























