 京都大学の研究グループは,金の微粒子を用いて細胞内に遺伝子を運び込み,数秒の光刺激で狙った細胞に好きなタイミングで遺伝子発現を誘導する方法を開発した(ニュースリリース)。
京都大学の研究グループは,金の微粒子を用いて細胞内に遺伝子を運び込み,数秒の光刺激で狙った細胞に好きなタイミングで遺伝子発現を誘導する方法を開発した(ニュースリリース)。
遺伝子発現とは,遺伝子が持つ情報に基づいてタンパク質分子が合成されることで,いわば「情報」を実際の「生命現象」に変える現象。遺伝子発現を操作することは生命現象の分子メカニズムを理解するために非常に重要で,複雑に構成された生体組織の中で,任意の細胞に任意のタイミングで,特定の遺伝子発現を誘導する技術が求められている。
遺伝子発現を誘導する一つの方法として,生体が熱ストレスに反応する機構を利用し,42℃前後の高温刺激を与えて誘導する方法は,以前より確立されていた。狙った細胞でのみ温度を上げる方法として,従来細胞内の水分子をレーザー照射で直接加熱する手法が考案されていたが,適切な温度で安定的な熱刺激を与えることが困難だった。
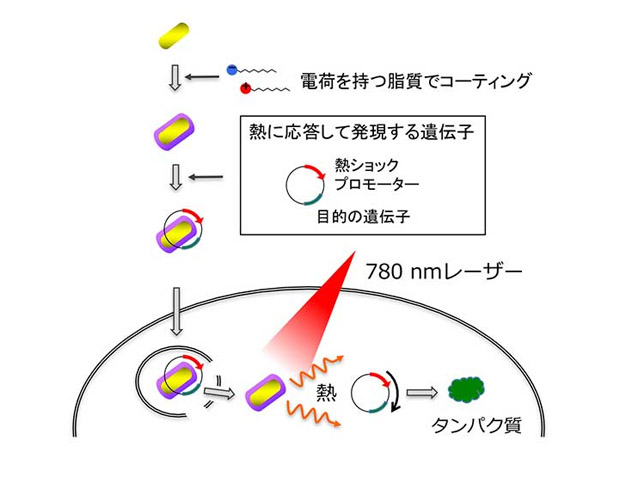
この問題を解消するため,研究グループは,金ナノロッドという約50nmのナノ粒子を用いた。金ナノロッドは光を吸収して熱を発生させることや,生体適合性が高いことで知られている。
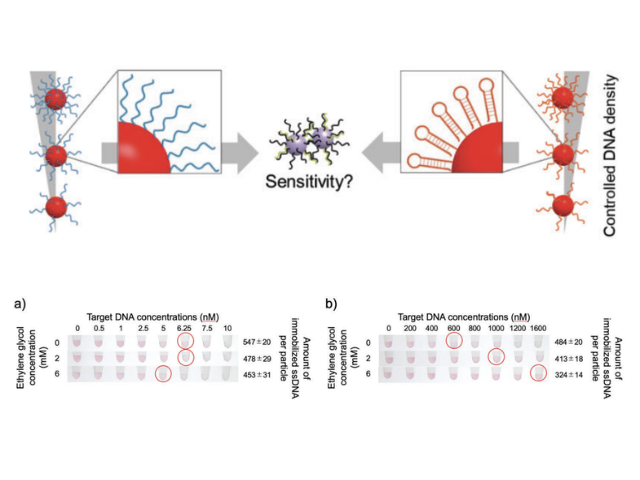
まず,熱に反応して発現する蛍光タンパク質遺伝子を作成した。そして,金ナノロッドに特殊なコーティングを施すことでこの遺伝子を吸着させた上で,細胞内に導入した。そこで,細胞に近赤外レーザー光を照射すると,照射した細胞内の温度が上昇し,照射中は一定の温度に保たれることがわかった。また,レーザー光の密度を調整することで細胞内の温度を調整することが可能で,遺伝子発現の誘導に必要な照射時間も大きく短縮された。
この手法を用いることにより,わずか数秒のレーザー光照射で,1細胞単位で任意の細胞だけに,任意のタイミングで目的の遺伝子発現を誘導することができた。また,応用的な試みとして,「TRAIL分子」という,がん細胞と結びつくことでそのがん細胞を殺す機能を持つタンパク質を,光照射による熱刺激で発現させ,周囲のヒトがん細胞が細胞死する現象も確認した。
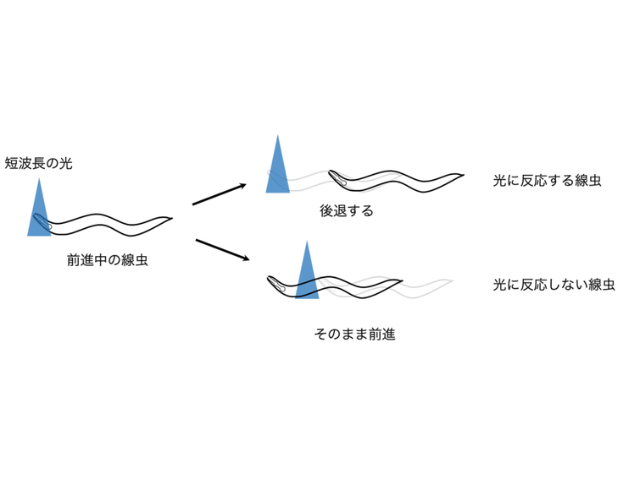
これまでにUV光などの短波長光刺激で遺伝子発現誘導する系が開発されていたが,光毒性が低く,より生体深部まで届く長波長光を用いたこの実験系は,組織などの細胞集団における遺伝子操作と機能解析により適しているという。金ナノロッド粒子を生体の標的器官で細胞導入する手法も開発されており,将来的にはがんなど様々な難病の安全な遺伝子治療への応用が期待されるとしている。