 京都大学の研究グループは,ナノメートルサイズの金粒子を使って,痛みを感知する神経細胞を光で活性化する手法を開発することに成功した(ニュースリリース)。
京都大学の研究グループは,ナノメートルサイズの金粒子を使って,痛みを感知する神経細胞を光で活性化する手法を開発することに成功した(ニュースリリース)。
ヒトが痛みを感じるとき,ある種の神経細胞が活性化している。その神経細胞の細胞膜上にあるTRPV1というイオンチャネルが痛みに繋がるさまざまな刺激(熱,酸,カプサイシンなど)を感知し,カルシウムイオンなどを細胞内に流入させることで痛みを伝達する。
TRPV1は神経痛や脳腫瘍の病原として知られており,神経細胞のTRPV1を望みの場所・時間で活性化できれば,身体に負担の少ない治療法になる可能性があるが,その方法は知られていなかった。
今回の研究では,ナノメートルサイズの棒状の金(金ナノロッド,以下AuNR)を用いた。AuNRは人体に最も影響の少ない近赤外光を吸収し,発熱したり,発光したりするなど,様々な応答性を示す。
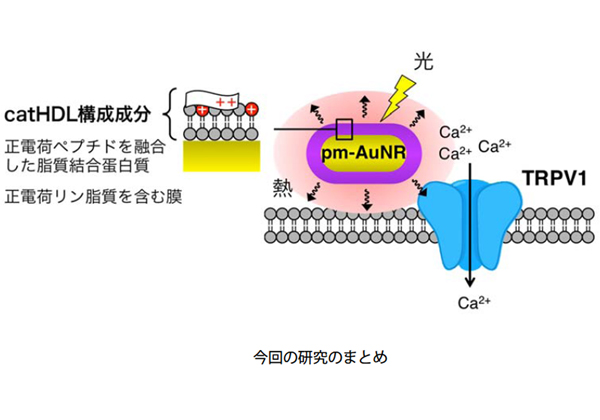
そこでこのAuNRをTRPV1近傍に輸送し,光照射による発熱作用を利用してTRPV1を活性化することを試みた。AuNRをTRPV1の存在する細胞膜に安全に輸送するには,慎重なAuNR表面処理が必要となる。そこで生体材料(高比重リポ蛋白質,以下HDL)を独自に改変してAuNRの表面処理に利用してみると,TRPV1を発現する細胞の細胞膜に多量のAuNRが膜ダメージを与えることなく輸送されることを発見した。
この細胞に780nmのレーザー近赤外光を照射すると,細胞膜近傍でのみ温度が上昇し,TRPV1の活性化を介してカルシウムイオンの流入がおきた。マウス脊髄から採取した痛みを感知する後根神経節細胞を用いても同様の結果が得られ,生理的条件下でも本手法は機能することがわかった。
今回の手法によって,神経細胞に人為的に「痛み」を伝達することが可能となった。今回用いた金粒子は,小分子化合物に比べて,局所投与部位に留まる性質がある。今後,この金粒子を疾患部位に局所投与して近赤外光照射するという新たな光治療法の開発などにより,細胞機能をリモートコントロールする新しい技術としてだけでなく,神経痛・脳腫瘍などの光治療法として期待されるという。
関連記事「基生研ら,2光子イメージングを用いて動物が1個の神経細胞の活動を意志で操作できることを証明」「名大ら,慢性疲労症候群モデル動物に生じる異常な痛みを抑えることに成功」






























