 産業技術総合研究所(産総研)は,フランス国立科学研究センター(CNRS),東北大学は共同で,生体透過性の高い近赤外レーザにより熱と活性酸素種を発生する有機色素とカーボンナノホーン(CNH)からなる分子複合体(ナノモジュレーター)を作製し,この分子複合体を用いて生きた細胞の機能を操作できる新たな光制御技術を開発した(ニュースリリース)。
産業技術総合研究所(産総研)は,フランス国立科学研究センター(CNRS),東北大学は共同で,生体透過性の高い近赤外レーザにより熱と活性酸素種を発生する有機色素とカーボンナノホーン(CNH)からなる分子複合体(ナノモジュレーター)を作製し,この分子複合体を用いて生きた細胞の機能を操作できる新たな光制御技術を開発した(ニュースリリース)。
近年,オプトジェネティクス(光遺伝学)を代表とする光を活用した細胞機能制御技術に注目が集まっている。オプトジェネティクスを用いると,光のスイッチを切り換えるだけで細胞同士の接続や特定の細胞集団の機能を操作できるため,未知の細胞ネットワークを解き明かし,病気の治療にも役立つと期待されている。
しかし,この技術は基本的に,紫外光や可視光などの生体透過性の低い光を用いるため,生体深部にある細胞の機能を制御できない。また,ウイルスを用いて遺伝子改変をな行う必要があるため,医療への応用は難しいという課題があった。
CNHは生体透過性の高い近赤外の波長領域(700~1100nm)のレーザにより容易に発熱する。今回開発したナノモジュレーターは,CNH表面に水溶性の近赤外蛍光色素(IRDye800CW)と水溶性のジアミノトリエチレングリコールを化学修飾してある。CNHの光発熱特性を最大限に発揮させるには,CNHを凝集させずに水などにナノレベルで分散させる必要があるが,通常CNHは水などに分散させようとしても,そのままでは粒状に凝集してしまう。今回,表面の水溶性分子により,開発したナノモジュレーターの水中での分散安定性は高く,凝集物の形成は観察されなかった。
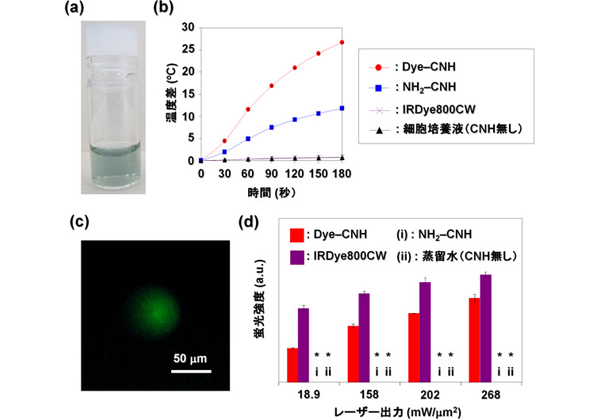
また,IRDye800CWとジアミノトリエチレングリコールの両方を化学修飾したCNH(Dye-CNH)分散液,ジアミノトリエチレングリコールだけを化学修飾したCNH(NH2-CNH)分散溶液,IRDye800CWだけの溶液,細胞培養液のそれぞれに波長800nmのレーザ光を照射したところ,Dye-CNH分散液で最大の温度上昇が見られた。NH2-CNH分散液では温度上昇するもののDye-CNHよりも小さかった。
一方,IRDye800CWだけの溶液,細胞培養液では,温度はほとんど上昇しなかった。Dye-CNH分散液が最大の温度上昇を示したのは,CNHの水中分散性,光発熱特性,近赤外光を吸収したIRDye800CWからCNHへのエネルギー移動や電子移動に伴う光発熱特性の増強効果によると考えられる。
IRDye800CWなどの多くの近赤外蛍光色素は,近赤外光を照射すると活性酸素種を発生することが知られている。Dye-CNH分散液に,活性酸素種が存在すると緑色の蛍光を発する色素を溶解させ,近赤外レーザを照射したところ蛍光顕微鏡により緑色蛍光が観察できた。
さらに,Dye-CNH分散液に加えてNH2-CNH分散液,IRDye800CWだけの溶液,蒸留水のそれぞれに蛍光色素を溶解させ,レーザを照射して蛍光顕微鏡により蛍光強度を測定したところ,Dye-CNH分散液とIRDye800CW溶液にだけレーザ出力に応じた強度の緑色蛍光が観察された。
これらは,今回開発したナノモジュレーター,Dye-CNHは,近赤外レーザ光によって効果的に熱と活性酸素種を発生することを示している。活性酸素種は,細胞内外へのイオンの出し入れに関わるタンパク質の活性を制御することで,ストレス,ホルモン伝達,免疫応答といった生命活動に欠かせないプロセスに関与しているため,ナノモジュレーターによる細胞機能制御が期待できるという。
今回開発したナノモジュレーターを用いて,細胞内へのカルシウムイオンの流入挙動を観測するため,マウス神経芽細胞腫とラット神経のハイブリッド細胞(ND7/23),マウスマクロファージ(RAW264.7),ヒト子宮頚部癌細胞(HeLa)に,ナノモジュレーターを取り込ませた。細胞内には,カルシウムイオンと結合すると緑色蛍光を発する指示薬も入れた。808nmの近赤外レーザを照射し,蛍光顕微鏡により観測したところ,3種類すべての細胞が効果的に蛍光を発光することから,ナノモジュレーターによりカルシウム流入が制御できることがわかった。
また,ナノモジュレーターを細胞内に導入したラット脊髄後根神経節(DRG)に785nmのレーザを照射し,パッチクランプ法によって細胞膜に流れる電流を測定したところ,レーザ出力に対応した電流の変化が見られ,ナノモジュレーターによる細胞膜の電流の制御の可能性も示された。
今回開発した技術では,生体透過性の高い近赤外光を利用するため,従来は不可能であった生体深部の細胞機能制御が可能と考えられるという。また,ウイルスを用いた遺伝子操作を必要としないので,例えば,ワイヤレス,ウイルスフリーで脳深部の特定領域の細胞を活性化させるなど,光を用いた細胞機能制御技術の性能を向上でき,さらに医療応用の可能性も高めることが期待できる。
研究グループは今後,この技術を応用して,単一の細胞レベルでの細胞機能解析技術を構築していく予定。また,パーキンソン病やアルツハイマー病などの脳疾患に関わる新しい治療法につながる周辺コア技術の開発にも取り組むとしている。
関連記事「東大,光によるグルタミン酸刺激と光遺伝学を用いてドーパミンの脳内報酬作用機構を解明」「OIST,「辛抱強さ」はセロトニンによって促進されることを光遺伝学で発見」「理研,神経軸索の集団的な伸長を支える分子メカニズムを蛍光観察により解明」「理研,「嫌な記憶」と「楽しい記憶」を光で書き換えることに成功」





























