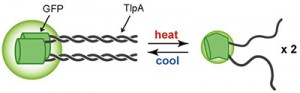
京都大学地球環境学堂教授の森泰生氏らの研究グループは、遺伝子工学的な手法を用いて、細胞内および細胞内小器官の温度計測を可能とする温度センサタンパク質を開発し、世界で初めて生体の恒常性を担う熱産生機構の可視化に成功した。
温度センサtsGFPを用いることで、熱産生組織として考えられていた褐色脂肪細胞からの熱産生の可視化に成功した。従来は、酸素消費などの間接的な状況証拠から褐色脂肪細胞が熱産生に関わると考えられてきたが、この研究ではミトコンドリアに発現する温度センサー(tsGFP1-mito)を用いることで、褐色脂肪細胞内のミトコンドリアから熱産生が行なわれていることを初めて直接的に示した。
また、小胞体に発現する温度センサ(tsGFP1-ER)を用いることで、非ふるえ熱としての寄与で意見が分かれていた筋細胞の小胞体からの熱産生の可視化にも成功し、筋細胞も熱産生を行なうことを直接的に証明した。これらの熱産生細胞は、肥満が問題となっている欧米を中心に、新たな肥満解消方法の標的として着目されている。
なぜなら、体内のエネルギーを熱の発散として消費できれば、新たなダイエットになるからである。しかし、これまでは熱産生組織からの熱産生を直接的に評価できる方法が皆無であり、熱産生を促す創薬の開発は困難とされてきた。一方、この研究成果(細胞内温度センサの開発)は、熱産生を直接的に評価できる方法となり得るので、肥満解消薬の開発が加速すると期待される。
詳しくはこちら。