東京大学大学院工学系研究科マテリアル工学専攻教授の片岡一則氏らの研究グループは,遺伝子導入の効率と選択性に優れた新規デリバリーシステムとして,三層構造の高分子ミセルをベースとした光応答性ナノマシンを構築した。
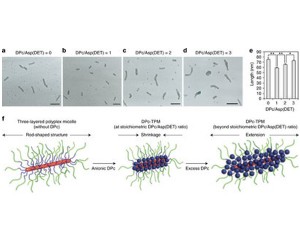
開発した全身投与型光応答性ナノマシンは,トリブロック共重合体,DNA(標的細胞に導入する遺伝子),光増感剤が水中で自動会合することによって形成され,親水性の外殻層,光増感剤が搭載された中間層,DNAを内包した内核層という三層の機能性ナノコンパートメントから構成される。
静脈に注射されたナノマシンは,最初に血液と接し,この時点でナノマシンに血液成分が吸着すると,血栓形成などの副作用に繋がる。このナノマシンは親水性外殻層によって,このような血液成分の吸着を抑制することが可能。
また,がんの血管では,正常な血管と比べて透過性が亢進していることから,ナノマシンはこの透過性を利用して血流からがん組織に集積することができる。さらに,ナノマシンはがん細胞に取り込まれ,エンドソーム・リソソーム内に局在する。
効率的な遺伝子の導入には最終的にDNAを核まで送達する必要があるため,まずエンドソーム・リソソームから細胞質に移行する必要がある。このナノマシンは,エンドソーム・リソソーム内の酸性環境に応答して光増感剤を放出する。ここに光を照射することで,エンドソーム・リソソーム膜を不安定化させ,ナノマシンの細胞質への移行を促進できる。
その結果,光を照射した標的細胞においてのみDNAを核まで効率的に送達することが可能となり,その遺伝子導入効率を,光を当てなかった場合と比較して100倍以上上昇させることに成功した。
さらに,開発したナノマシンを皮下に腫瘍のあるモデルマウスの全身に投与し,固形がんに光を照射することで,光が照射された固形がんに選択的に目的の遺伝子が導入できることを世界で初めて示した。
この遺伝子デリバリーシステムは,ウイルスベクター等の従来の遺伝子導入技術と比較して安全性と選択性に優れ,全身投与が可能であることから,がんや動脈硬化などのさまざまな難治性疾患の遺伝子治療への応用が期待される。
詳しくは東京大学 プレスリリースへ。